第二章化学物质及其变化[考纲解读]1
了解分子、原子、离子和原子团等概念的含义
理解物理变化与化学变化的区别与联系
理解混合物和纯净物、单质和化合物、金属和非金属的概念
理解酸、碱、盐、氧化物的概念及其相互关系
了解胶体是一种常见的分散系;了解溶液和胶体的区别
了解电解质的概念,了解强电解质和弱电解质的概念
理解电解质在水溶液中的电离以及电解质溶液的导电性
了解离子反应的概念、离子反应发生的条件,能正确书写离子方程式,并能进行有关计算
掌握常见离子的检验方法
能正确判断常见离子在溶液中能否大量共存
了解氧化还原反应的本质
了解常见的氧化还原反应
掌握常见氧化还原反应的配平和相关计算
第4讲物质的组成、分类及性质一、物质的组成元素、物质及微粒间的关系(1)宏观上物质是由元素组成的,微观上物质是由分子、原子或□离子构成的
①元素:具有□相同核电荷数的一类原子的总称
②原子是□化学变化中的最小微粒
分子是□保持物质化学性质的最小微粒,一般分子由原子通过共价键构成,但稀有气体是单原子分子
离子是带电荷的原子或原子团
(2)元素与物质的关系(3)元素在物质中的存在形态①游离态:元素以□单质形式存在的状态
②化合态:元素以□化合物形式存在的状态
(4)同素异形体二、物质的分类1.常见的分类方法(1)交叉分类法——从不同角度对物质进行分类(2)树状分类法——按不同层次对物质进行逐级分类,各层之间属于包含关系2.分散系(1)概念:□把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系
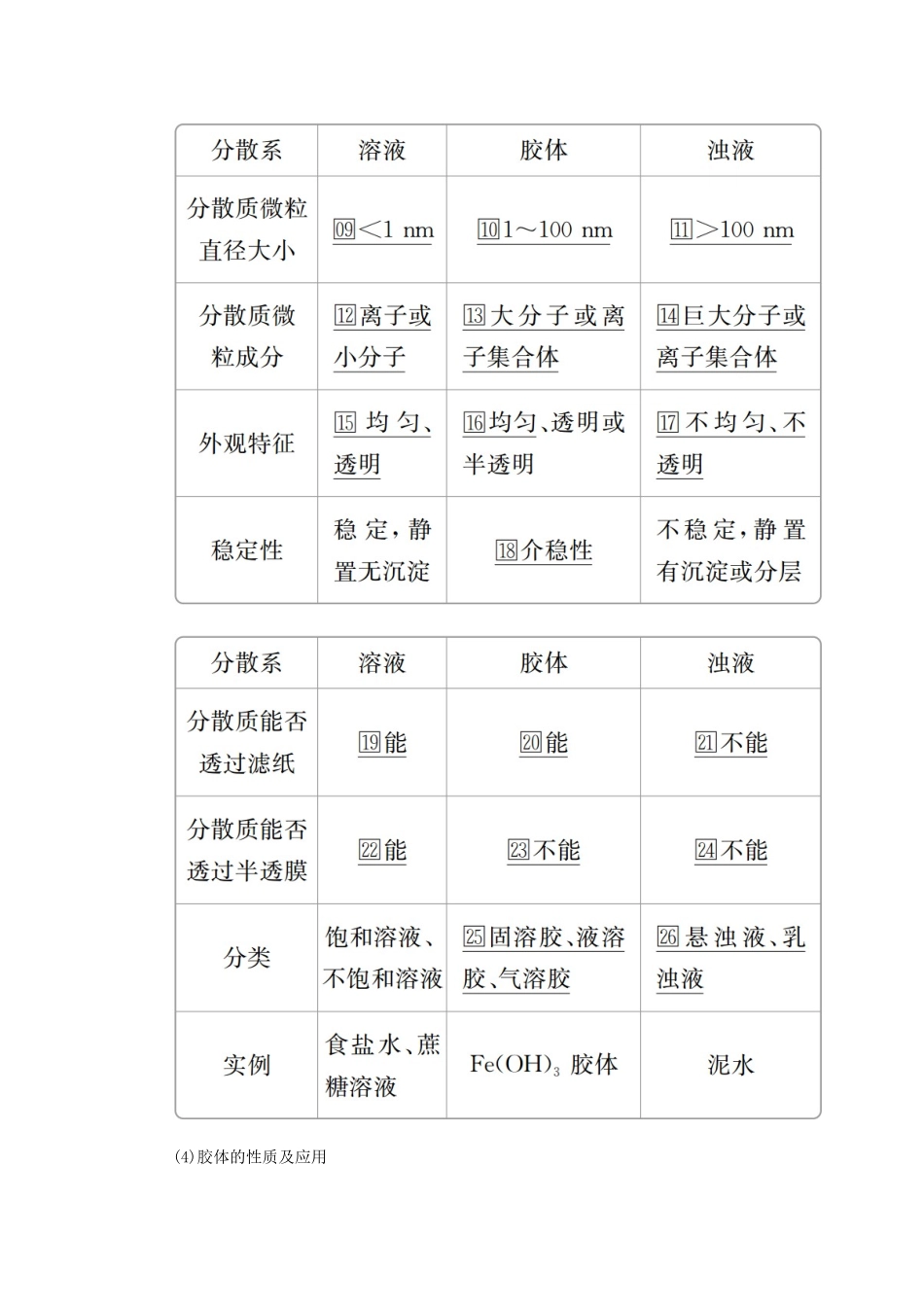
(2)分类:按照分散质粒子直径的大小(3)三种分散系比较(4)胶体的性质及应用①丁达尔效应可见光束通过胶体时,在入射光侧面可看到□光亮的通路,这是胶体粒子对光线散射而形成的,可用此性质来鉴别溶液和胶体
②聚沉a.概念:使胶体粒子聚集形成沉淀析出的