几种重要金属化合物(第3课时)【学习目标】1
掌握铁的氧化物、氢氧化物的主要性质
掌握Fe3+的检验、氧化性及Fe2+与Fe3+的相互转化
【学习过程】人类早在6000年前就开始利用铁,2000年前人类发明了从矿石里冶铁的方法
我国在春秋时期就开始冶铁、战国时期就开始炼钢
钢铁一直广泛地应用人类生活的方方面面
铁的氧化物2.铁的氢氧化物:(1)制备:实验步骤实验现象化学方程式在2支试管晨分别加入少量FeCl3和FeSO4溶液,然后滴入NaOH溶液,观察并描述发生的现象FeCl3溶液中生成红褐色沉淀FeCl3+3NaOH=Fe(OH)3↓+3NaClFeSO4溶液中生成白色沉淀,后又迅速转变为灰绿色,最后生成红褐色FeSO4+2NaOH=Fe(OH)2↓+Na2SO44Fe(OH)2+O2+2H2O=4Fe(OH)3温馨提示:实验室制备氢氧化亚铁时,因氢氧化亚铁在空气中极易与氧气、水反应生成氢氧化铁,更要注意隔绝空气
其方法是:①亚铁盐需新制(用足量铁与稀硫酸反应或还原氯化铁溶液);②将所用氢氧化钠溶液煮沸以赶尽溶于其中的空气(O2);③使用长滴管吸入氢氧化钠溶液后将滴管伸至氯化亚铁溶液的液面以下,慢慢挤压乳胶头使氢氧化钠与氯化亚铁接触
(2)性质:化学式Fe(OH)2Fe(OH)3颜色状态白色固体红褐色固体溶解性不溶于水不溶于水稳定性易被氧化Fe(OH)3△Fe2O3+H2O4Fe(OH)2+O2+2H2O=4Fe(OH)3与H+反应Fe(OH)2+2H+=Fe2++2H2O(氧化性酸生成Fe3+)Fe(OH)3+3H+=Fe3++3H2O转化关系4Fe(OH)2+O2+2H2O=4Fe(OH)33
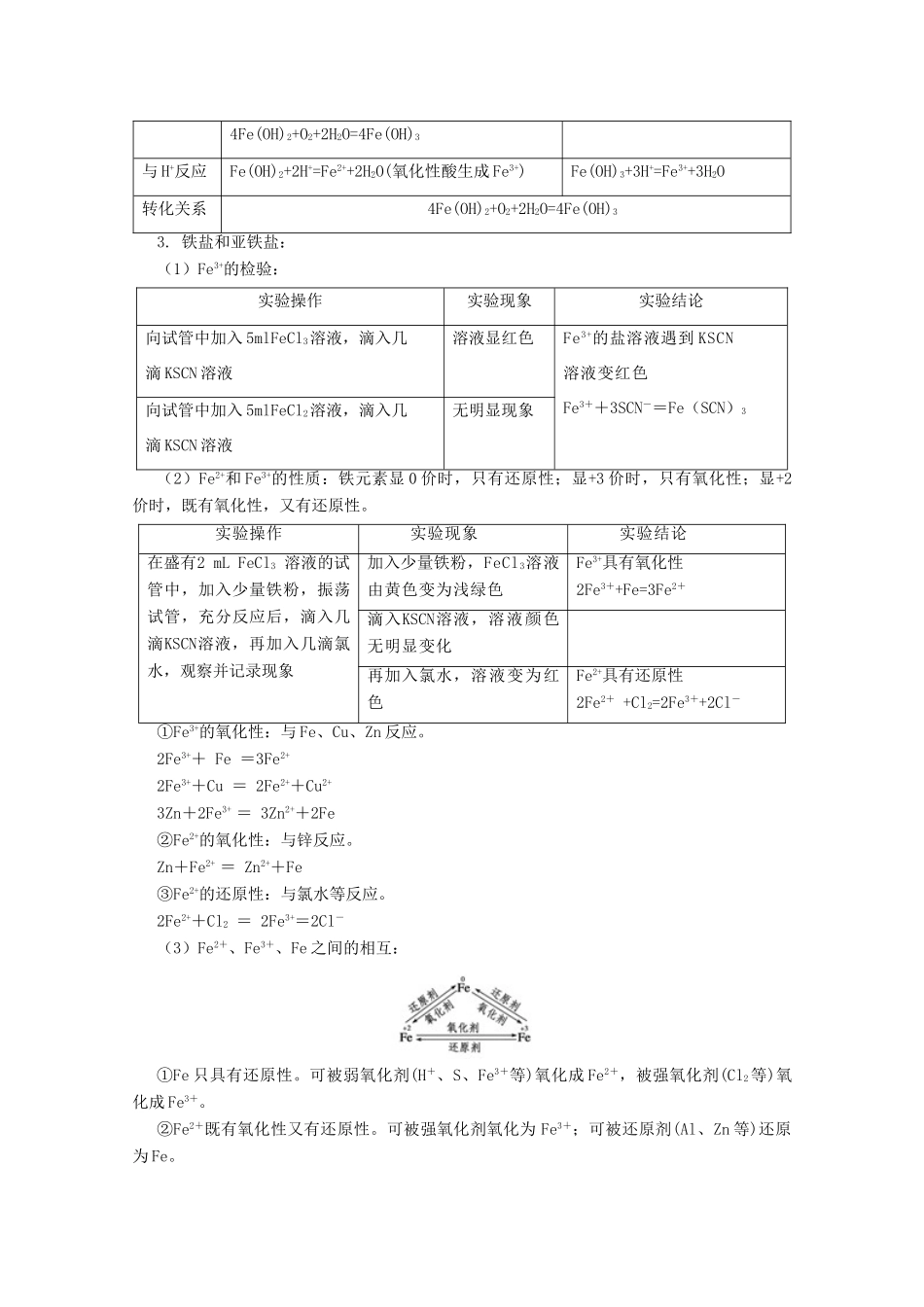
铁盐和亚铁盐:(1)Fe3+的检验:实验操作实验现象实验结论向试管中加入5mlFeCl3溶液,滴入几滴KSCN溶液溶液显红色Fe3+的盐溶液遇到KSCN溶液变红色Fe3