第2课时元素的性质与原子结构学习目标1
了解原子结构与元素性质的关系
初步学会总结元素递变规律的能力
学习过程一、碱金属元素1
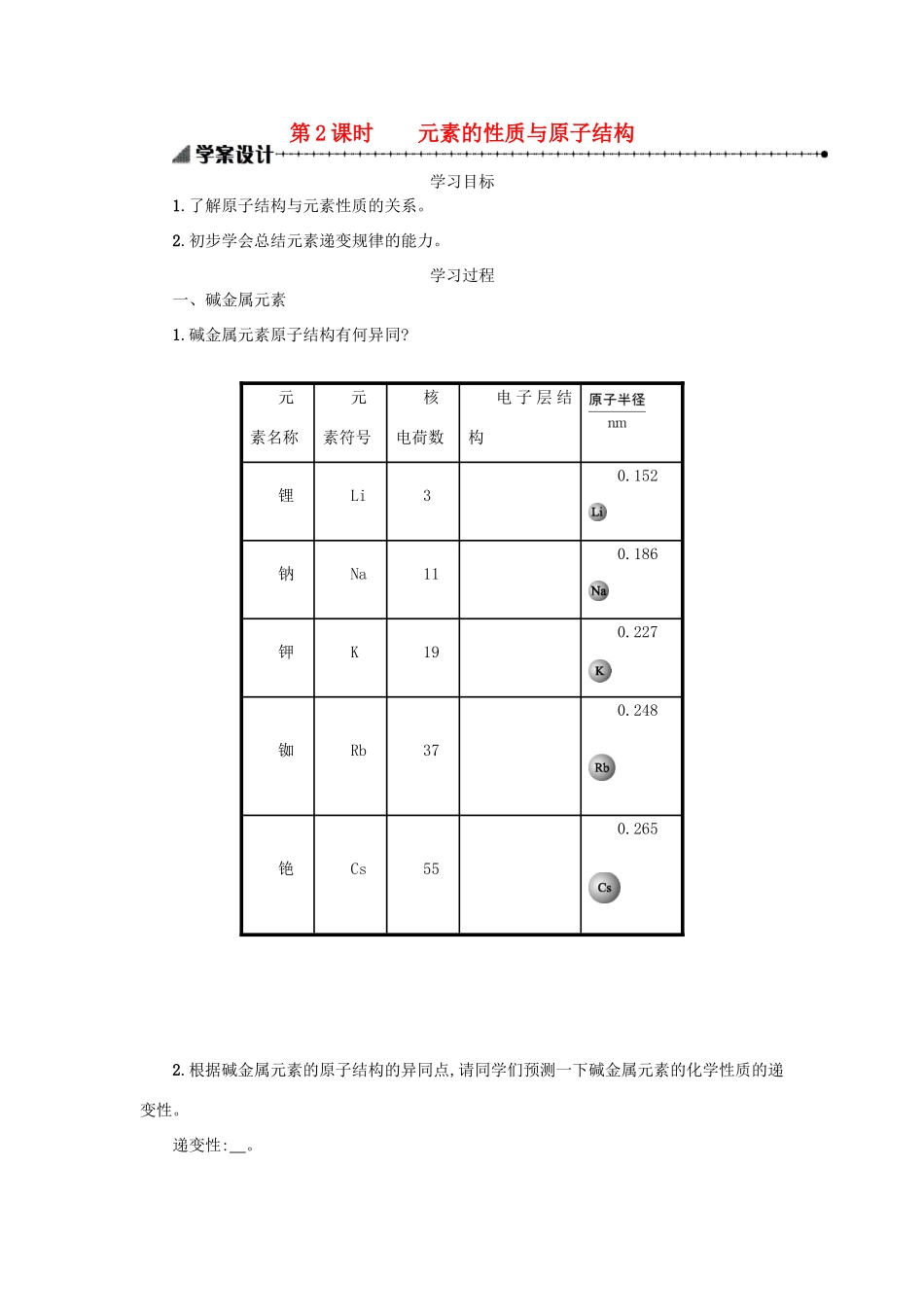
碱金属元素原子结构有何异同
元素名称元素符号核电荷数电子层结构锂Li30
152钠Na110
186钾K190
227铷Rb370
248铯Cs550
根据碱金属元素的原子结构的异同点,请同学们预测一下碱金属元素的化学性质的递变性
[实验](1)Na、K与氧气反应对比实验,先后取一小块钾和一小块钠,擦干表面的煤油后分别放在石棉网上加热,观察现象
(2)分别取绿豆大的钾、钠擦干表面的煤油后分别放在两个水槽中与水反应,并在水中滴入几滴酚酞溶液
写出下列反应的化学方程式:Li+O2——Na+O2——K+O2——Li+H2O——Na+H2O——K+H2O——归纳总结:3
阅读课本P7表11碱金属的主要性质,归纳总结碱金属的物理性质及递变规律
[练习]下列关于铯及其化合物的说法中,不正确的是()A
氢氧化铯是一种强碱,易溶于水B
铯与水反应十分剧烈,甚至发生爆炸C
碳酸铯用酒精灯加热可以生成氧化铯和CO2D
硫酸铯、碳酸铯、硝酸铯都是易溶于水二、卤族元素1
(1)根据卤素原子的结构来推测其性质上的相似性与递变性
(2)根据卤族元素的结构特点和必修1所学氯气的性质,归纳总结卤族元素的通性
阅读课本P8,根据资料卡片卤族单质的物理性质总结其物理性质的递变规律
阅读课本P8表卤素单质与氢气反应,总结卤素单质化学性质的递变规律
卤素单质的置换反应[实验1]将少量新制的饱和氯水分别注入盛有NaBr溶液和KI溶液的试管中,用力振荡后,再注入少量四氯化碳,振荡
观察四氯化碳层和水层的颜色变化
发生反应的化学方程式:
[实验2]将少量的溴水注入盛有KI溶液的试管中,用力振荡后,再