第一课时离子键学习目标:1
通过氯化钠的形成理解离子键的概念及本质和形成条件
通过实例了解离子化合物的概念,能识别典型的离子化合物
能熟练地用电子式表示物质的组成及离子化合物的形成过程
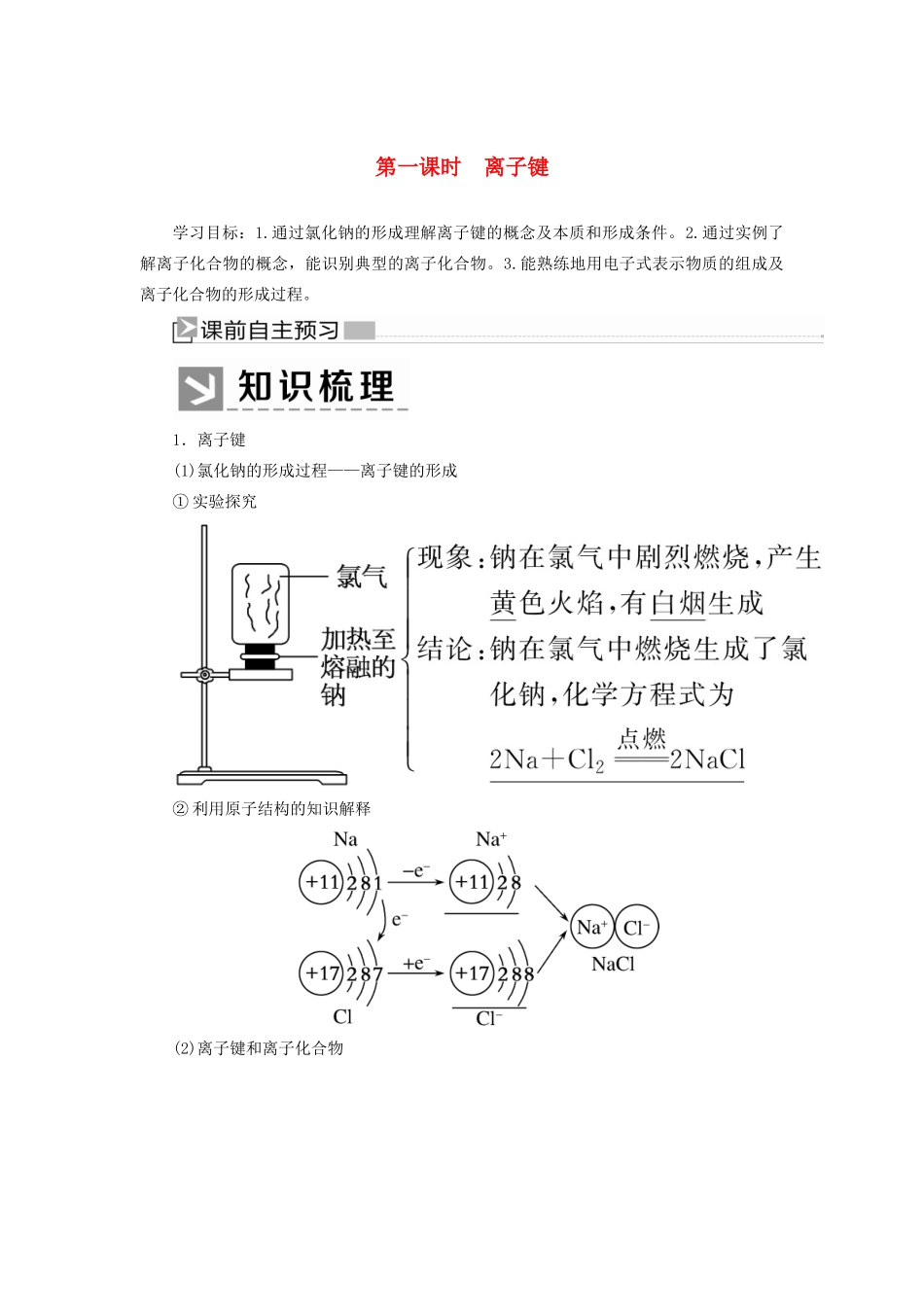
1.离子键(1)氯化钠的形成过程——离子键的形成①实验探究②利用原子结构的知识解释(2)离子键和离子化合物2.电子式(1)概念在元素符号周围用“·”或“×”来表示原子的最外层电子(价电子)的式子
(2)电子式的书写①原子的电子式元素符号周围标明元素原子的最外层电子,每个方向不能超过2个电子
当最外层电子数小于或等于4时以单电子分布,多于4时多出部分以电子对分布
例如:镁原子:·Mg·;碳原子:·C·;氧原子:·O·;氖原子:
②简单阳离子的电子式简单阳离子是由金属原子失电子形成的,原子的最外层已无电子,故用阳离子的符号表示,例如:Na+、Li+、Mg2+、Al3+等
③简单阴离子的电子式不但要画出最外层电子数,而且还应用“[]”括起来,并在右上角标出“n-”以表示其所带的电荷
例如:氯离子[Cl]-、硫离子[S]2-
④复杂阴、阳离子的电子式复杂阴、阳离子要标明电子,用“[]”括上,并在“[]”右上角标明电性和电量,例如:⑤离子化合物的电子式氧化钙:Ca2+[O]2-、硫化钾:K+[S]2-K+
(3)用电子式表示下列物质的形成过程①NaCl:NaCl―→Na+[Cl]-
②MgBr2:BrMgBr―→[Br]-Mg2+[Br]-
1.判断正误(正确的打“√”,错误的打“×”)(1)阴、阳离子通过静电引力形成离子键()(2)离子化合物中一定含有金属元素()(3)由金属元素和非金属元素形成的化合物一定是离子化合物()(4)阴、阳离子间通过离子键一定能形成离子化合物()(5)NH4Cl属于离子化合物,其电子式为()[答案](1)×(2)×(3)×(4)√(5)×2.以