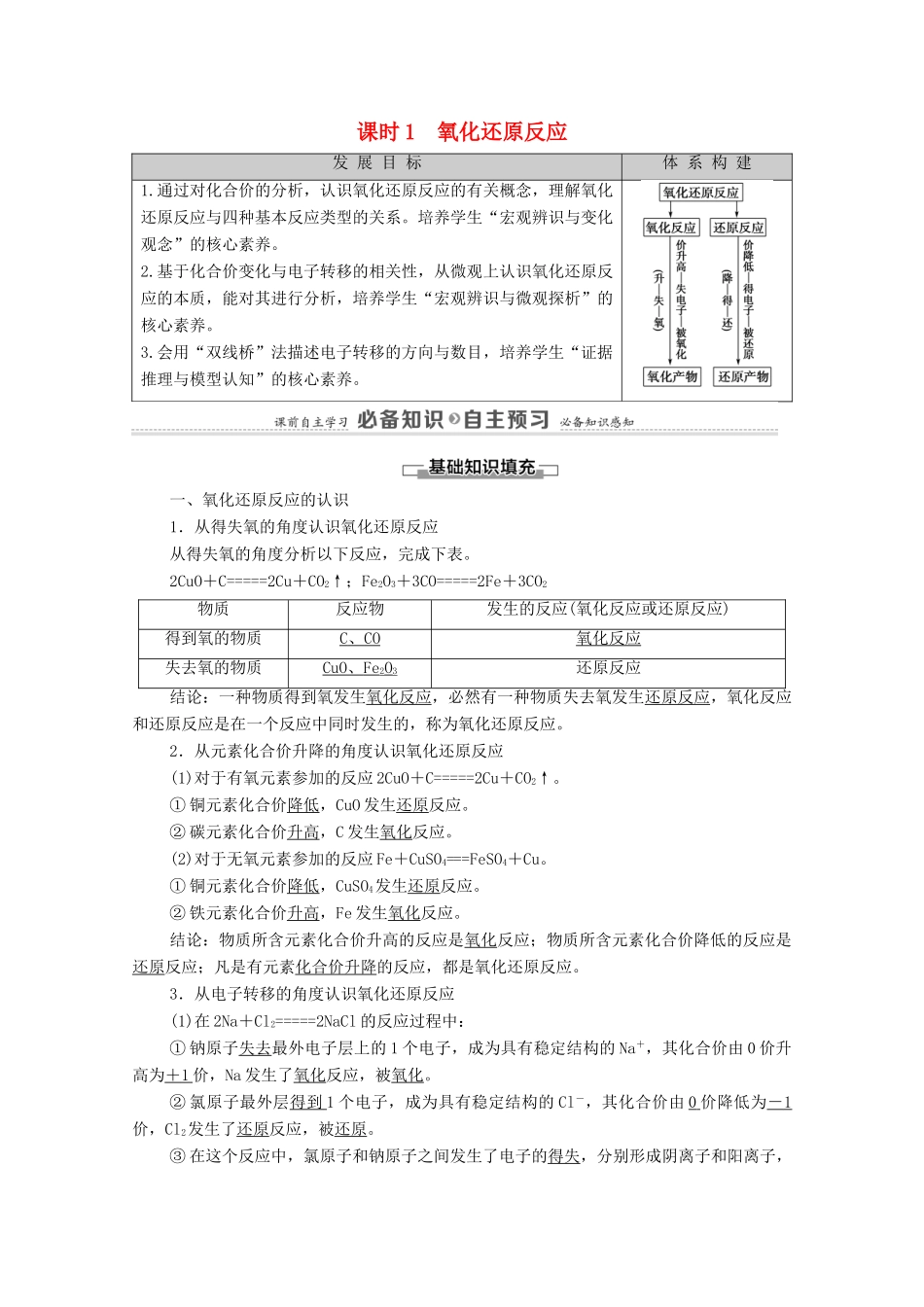
课时1氧化还原反应发展目标体系构建1
通过对化合价的分析,认识氧化还原反应的有关概念,理解氧化还原反应与四种基本反应类型的关系
培养学生“宏观辨识与变化观念”的核心素养
基于化合价变化与电子转移的相关性,从微观上认识氧化还原反应的本质,能对其进行分析,培养学生“宏观辨识与微观探析”的核心素养
会用“双线桥”法描述电子转移的方向与数目,培养学生“证据推理与模型认知”的核心素养
一、氧化还原反应的认识1.从得失氧的角度认识氧化还原反应从得失氧的角度分析以下反应,完成下表
2CuO+C=====2Cu+CO2↑;Fe2O3+3CO=====2Fe+3CO2物质反应物发生的反应(氧化反应或还原反应)得到氧的物质C、CO氧化反应失去氧的物质CuO、Fe2O3还原反应结论:一种物质得到氧发生氧化反应,必然有一种物质失去氧发生还原反应,氧化反应和还原反应是在一个反应中同时发生的,称为氧化还原反应
2.从元素化合价升降的角度认识氧化还原反应(1)对于有氧元素参加的反应2CuO+C=====2Cu+CO2↑
①铜元素化合价降低,CuO发生还原反应
②碳元素化合价升高,C发生氧化反应
(2)对于无氧元素参加的反应Fe+CuSO4===FeSO4+Cu
①铜元素化合价降低,CuSO4发生还原反应
②铁元素化合价升高,Fe发生氧化反应
结论:物质所含元素化合价升高的反应是氧化反应;物质所含元素化合价降低的反应是还原反应;凡是有元素化合价升降的反应,都是氧化还原反应
3.从电子转移的角度认识氧化还原反应(1)在2Na+Cl2=====2NaCl的反应过程中:①钠原子失去最外电子层上的1个电子,成为具有稳定结构的Na+,其化合价由0价升高为+1价,Na发生了氧化反应,被氧化
②氯原子最外层得到1个电子,成为具有稳定结构的Cl-,其化合价由0价降低为-1价,Cl2发生了还原反应,被还原