课时1物质的分类发展目标体系构建1
通过对生活实例的反思,提炼分类的意义和方法,并迁移至物质的分类,能对酸、碱、盐、氧化物概念进行描述,培养“宏观辨识”的化学素养
通过实例认识分散系、胶体,理解胶体的实质和重要性质,培养“宏观辨识与微观探析”的化学素养
通过Fe(OH)3胶体的实验制备和性质探究,培养“科学态度与科学探究”的化学素养
一、根据物质的组成和性质分类化学研究的基础:根据元素组成对物质进行分类是化学研究的基础
1.根据元素组成的物质种类(1)单质①元素组成:由同种元素组成的纯净物,每一种元素都可以形成单质,属于元素的游离态存在形式
②同素异形体:由同一种元素形成的几种性质不同的单质
如碳元素的三种常见同素异形体有金刚石、石墨、C60;O2与O3是氧元素的同素异形体;等等
(2)化合物微点拨:(1)由同种元素形成的物质不一定为纯净物
(2)任何元素之间不一定均能形成化合物
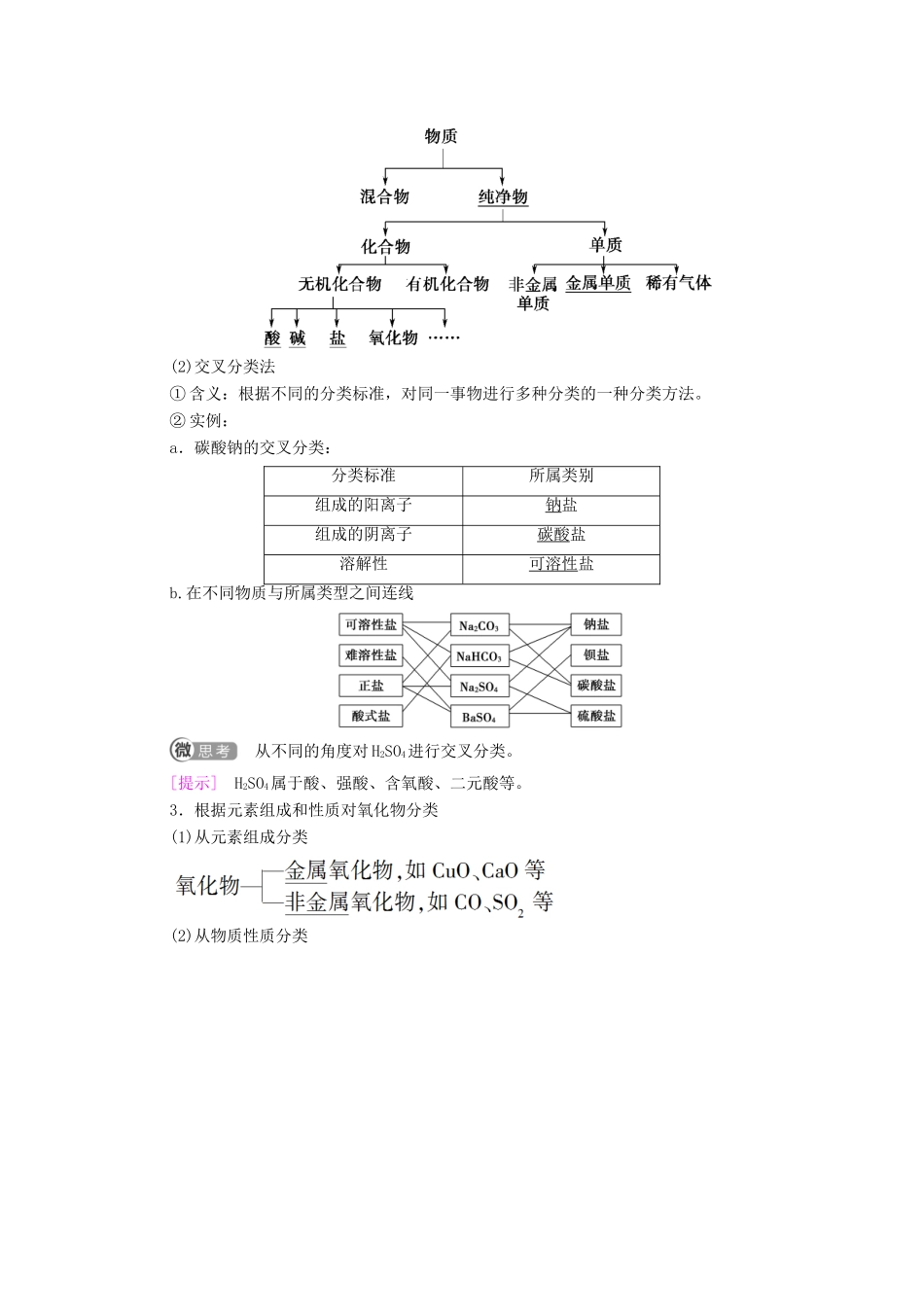
2.常见物质的分类方法(1)树状分类法①含义:根据物质的组成对物质进行分类的一种方法
②实例:根据物质的组成可对物质进行如下分类:(2)交叉分类法①含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法
②实例:a.碳酸钠的交叉分类:分类标准所属类别组成的阳离子钠盐组成的阴离子碳酸盐溶解性可溶性盐b
在不同物质与所属类型之间连线从不同的角度对H2SO4进行交叉分类
[提示]H2SO4属于酸、强酸、含氧酸、二元酸等
3.根据元素组成和性质对氧化物分类(1)从元素组成分类(2)从物质性质分类微点拨:(1)科学分类能够反映事物的本质特征
(2)分类不但适用于物质分类也适用于物质变化的分类,便于研究物质的性质
(3)运用分类,可以发现同类物质的共性及其变化规律,并预测物质的性质及可能发生的变化
二、分散系及其分类1.分散系(1)概念:化学上把一种(或多种)物质以粒子形式分散到另一种(或多种