第二节、元素周期律•分析归纳1到18号元素原子的核外电子排布、主要化合价、原子半径的变化规律
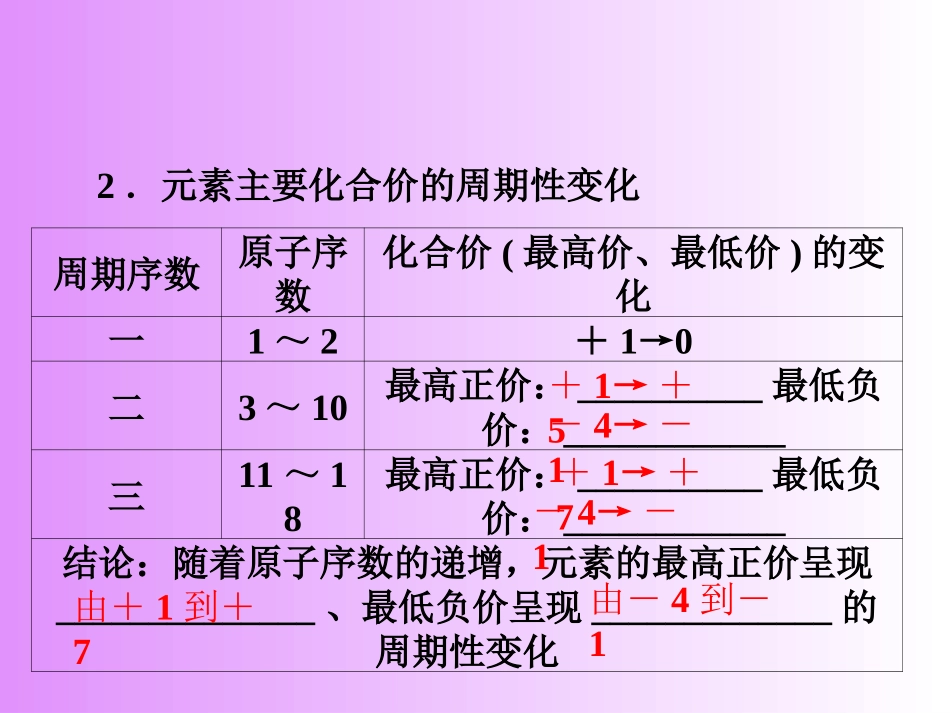
一、元素性质的周期性变化1.元素原子核外电子排布的周期性变化周期序数原子序数最外层电子的变化一1~21→2二3~10三11~18结论:随着原子序数的递增,元素原子核外电子的排布呈现_____________变化1→81→8周期性2.元素主要化合价的周期性变化周期序数原子序数化合价(最高价、最低价)的变化一1~2+1→0二3~10最高正价:__________最低负价:____________三11~18最高正价:__________最低负价:____________结论:随着原子序数的递增,元素的最高正价呈现______________、最低负价呈现_____________的周期性变化+1→+5-4→-1+1→+7-4→-1由+1到+7由-4到-13.元素原子半径的周期性变化周期序数原子序数最外层电子的变化一1~2二3~10三11~18结论:随着原子序数的递增,元素的原子半径呈现_____________变化大→小大→小周期性4
元素金属性与非金属性的周期性变化(1)Na、Mg、Al金属性强弱的比较(2)Si、P、S、Cl非金属性强弱的比较周期表中元素性质的变化规律项目同周期(从左到右)同主族(从上到下)最外层电子数由1逐渐增到7(第一周期由1到2)相同主要化合价最高正价+1→+7最低负价-4→-1最高正价相同(O、F除外)原子半径逐渐减小(稀有气体除外)逐渐增大项目同周期(从左到右)同主族(从上到下)得失电子能力得电子能力增强,失电子能力减弱得电子能力减弱,失电子能力增强单质的氧化性、还原性还原性减弱、氧化性增强氧化性减弱,还原性增强最高价氧化物对应水化物的酸碱性碱性减弱,酸性增强酸性减弱,碱性增强非金属氢化物的生成难易及稳定性生成由难到易,稳定性由弱到强生成由易到难,稳定性由