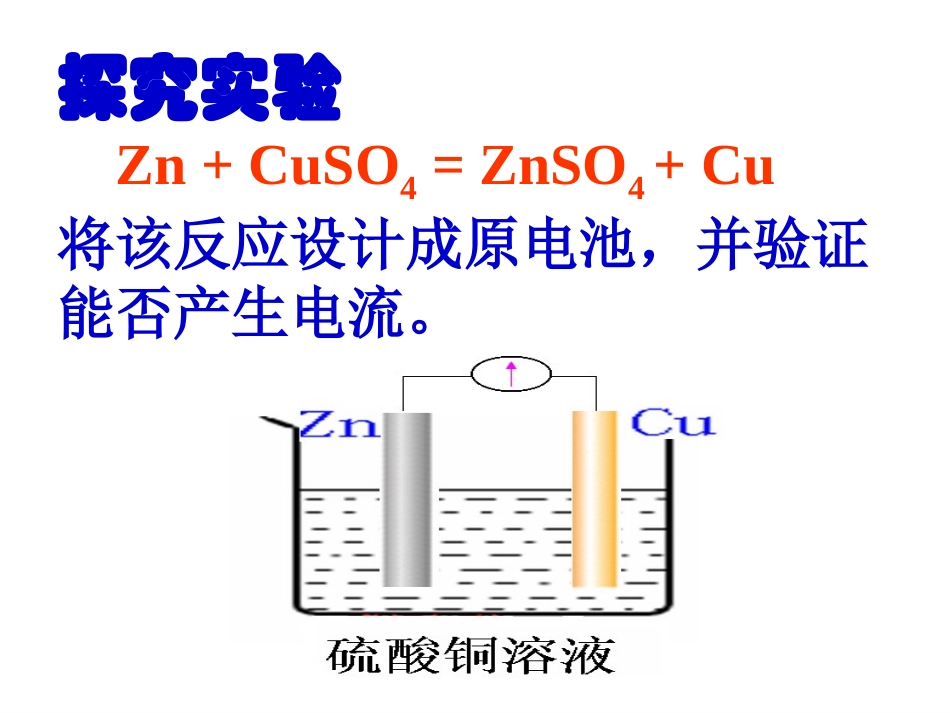
新课标人教版选修四化学反应原理第四章电化学基础第一节原电池授课教师:周伟探究实验Zn+CuSO4=ZnSO4+Cu将该反应设计成原电池,并验证能否产生电流
断开外电路,Zn也会和CuSO4直接反应,故不能长期保存
断开外电路,该原电池能否长期保存
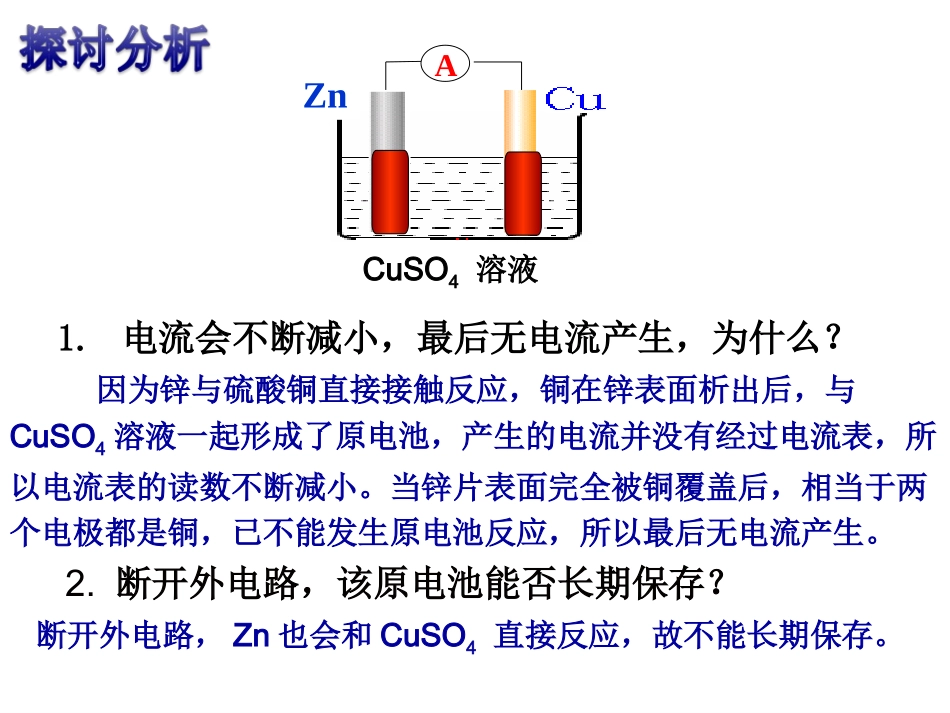
CuSO4溶液AZn1
电流会不断减小,最后无电流产生,为什么
因为锌与硫酸铜直接接触反应,铜在锌表面析出后,与CuSO4溶液一起形成了原电池,产生的电流并没有经过电流表,所以电流表的读数不断减小
当锌片表面完全被铜覆盖后,相当于两个电极都是铜,已不能发生原电池反应,所以最后无电流产生
CuCuZnZnZnSOZnSO44溶液溶液CuSOCuSO44溶液溶液A1
烧杯中加什么溶液
实验设计不与锌反应的溶液,一般加金属对应的盐溶液
安培表指针会偏转吗
怎样构成闭合回路
实验探究盐桥中通常装有含KCl饱和溶液的琼脂K+和Cl-在盐桥中能移动信息提示SO42-Zn2+e-e-SO42-Cu2+K+盐桥工作示意图CuZnK+Cl-K+Cl-K+Cl-K+Cl-K+Cl-Cl-K+K+Cl-K+K+K+Cl-Cl-K+Cl-Cl-Cl-★盐桥的作用:(1)形成闭合回路(2)平衡电荷1
有效避免了电极材料与电解质溶液的直接反应,增加了原电池的使用寿命2
能够产生持续稳定的电流,提高了原电池的使用效率使用了盐桥的原电池有什么优点
CCuFeCl3CuSO4利用反应:2FeCl3+Cu===2FeCl2+CuCl2分别设计出单液和双液原电池的装置图信息:现有材料只能让阳离子通过(阳离子交换膜);只能让阴离子通过(阴离子交换膜)ZnSO4溶液CuSO4溶液阴离子交换膜带离子交换膜的原电池“只有蓝天、没有雾霾”利用Cu+2Ag+=Cu2++2Ag反应,设计一个能产生持续、稳定电流的原电池装置,写出电极反应式,画出装置图