第一章《物质结构元素周期律》第三节化学键第一课时学科网【问题】NaCl固体导电吗
怎样才能使它导电
NaCl熔融(或溶于水)才能导电这说明钠离子和氯离子存在强烈的相互作用这种强烈的相互作用是什么
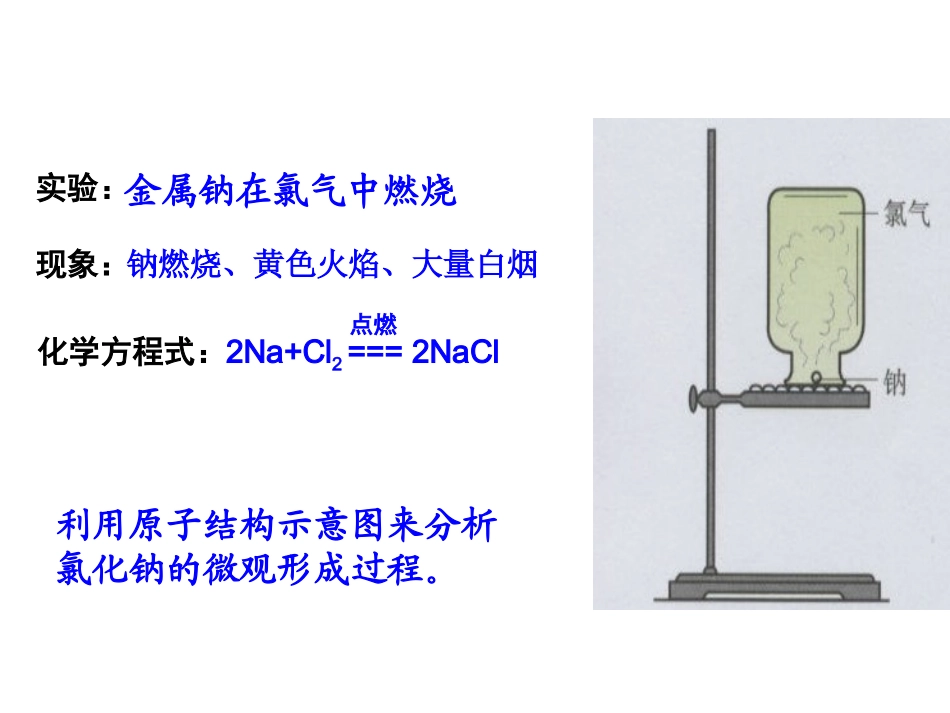
化学键点燃实验:化学方程式:钠燃烧、黄色火焰、大量白烟现象:2Na+Cl2===2NaCl利用原子结构示意图来分析氯化钠的微观形成过程
金属钠在氯气中燃烧2、理论探究形成概念Na+11812Cl+17872+1182+17882Na+Cl-Na和Cl2的反应1
概念:带相反电荷离子之间的相互作用称为离子键2
概念要点:成键微粒——阴、阳离子相互作用——静电作用(阴阳离子间的静电引力及电子间、原子核间的斥力)一、离子键思考思考哪些元素能形成离子键
活泼的金属元素(IA,IIA)和活泼的非金属元素(VIA,VIIA)之间容易形成离子键
学科网H元素周期表LiBe……NOFNaMgPSClKCaAsSeBrRbSrSbTeICsBaBiPoAtFrRa常见阳离子金属离子:Na+、Mg2+、Ca2+铵根离子:NH4+常见阴离子Cl-、S2-、OH-O2-CO32-、SO42-、NO3-离子化合物:含离子键的化合物
常见的离子化合物:强碱、大多数盐(AlCl3除外)、活泼金属氧化物、活泼金属氢化物1、原子的电子式:SClCa二、电子式电子式:在元素符号周围用小黑点·(或×)来表示原子的最外层电子的式子
写出下列原子的电子式钠原子镁原子碳原子氮原子Na×Mg××C××××N·····硫原子氯原子钙原子FO2-②阴离子的电子式:2、离子的电子式:①阳离子的电子式:一般用离子符号表示(NH4+除外)表示,只要在元素符号右上角标出“n+”电荷字样
一般用表示Rn-S2-写出下列阳离子的电子式钾离子镁离子钙离子K+Mg2+Ca2+写出下列阴离子的电子式氟离子氧离子硫离子ClNa3、离子化合物: