二、分散系及其分类1、分散系的概念把所得到的混合体系,叫做分散系
前者属于,称作,后者起的作用,称作
其实,初中我们学过的溶液就是一种分散系,其中溶质属于,溶剂属于
初中我们还学过悬浊液和乳浊液,它们也是分散系
例如泥水中的水是,泥土小颗粒是
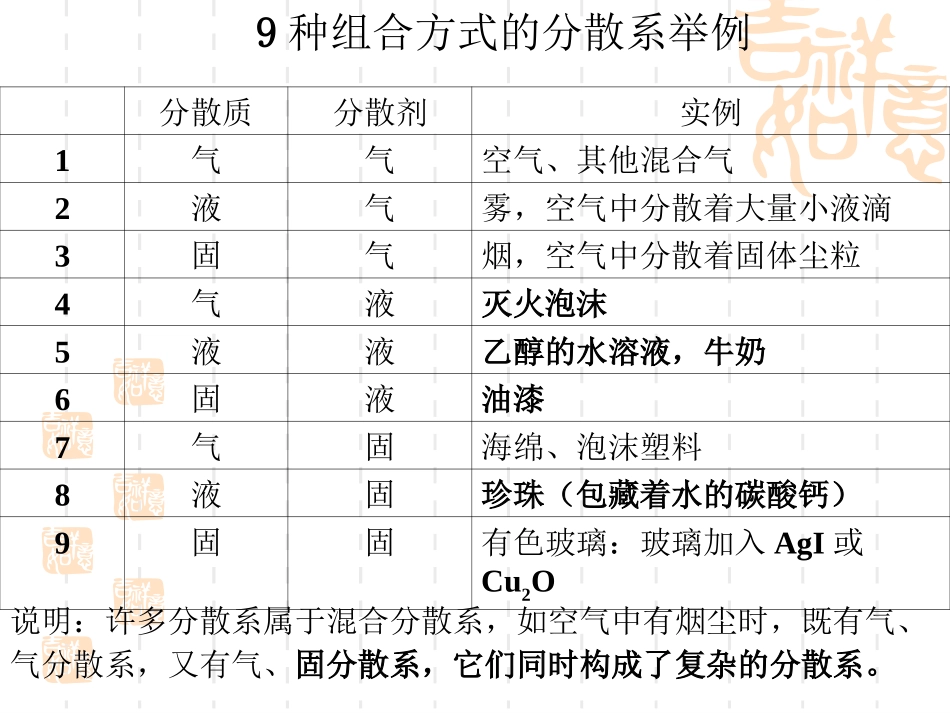
一种(或多种)物质分散在另一种(或多种)物质中被分散的物质分散质容纳分散质分散剂分散质分散剂分散剂分散质根据分散质与分散剂的状态,它们之间可以有9种组合方式:分散质分散剂气气液液固固9种分散系9种组合方式的分散系举例分散质分散剂实例1气气空气、其他混合气2液气雾,空气中分散着大量小液滴3固气烟,空气中分散着固体尘粒4气液灭火泡沫5液液乙醇的水溶液,牛奶6固液油漆7气固海绵、泡沫塑料8液固珍珠(包藏着水的碳酸钙)9固固有色玻璃:玻璃加入AgI或Cu2O说明:许多分散系属于混合分散系,如空气中有烟尘时,既有气、气分散系,又有气、固分散系,它们同时构成了复杂的分散系
分散系的分类分散系分散质粒子大小主要特征举例溶液100nm不稳定、不均一不透明泥浆水分散质粒子大小溶液胶体浊液当分散剂是水或其它液体时科学探究1、Fe(OH)3胶体的制备实验及胶体、溶液、浊液外观特征的比较:实验步骤:①取三个小烧杯,分别加入25ml蒸馏水、25mlCuSO4溶液和25ml泥水
②将烧杯中的蒸馏水加热至,向沸水中逐滴加入FeCl3饱和溶液,继续煮沸至,停止加热,即制得红褐色的
对比三种分散系:实验现象:
实验结论:FeCl3+3H2O=Fe(OH)3(胶体)+3HCl溶液属稳定的分散系,而浊液是不稳定的分散系
胶体则介于二者之间,在一定条件下能,属于
沸腾溶液呈红褐色Fe(OH)3胶体稳定存在介稳体系CuSO4溶液和Fe(OH)3胶体都很稳定,泥水会沉降,不稳定思考胶体为什么具有介稳性
原因一胶体粒子可以通过吸附离子而带有电荷,同种胶粒带同种电荷,