第三章水溶液中的离子平衡第三节盐类的水解第一课时2•水呈中性,是因为水中的H+的浓度与OH-的浓度相等;•酸呈酸性,是因为酸能够电离出H+而使溶液中的H+的浓度大于OH-的浓度;•碱呈碱性,则是由于碱能够电离出OH-而使溶液中的OH-的浓度大于H+的浓度的缘故
【知识回顾】思考:那盐溶液的酸碱性如何呢,是否一定是呈中性呢
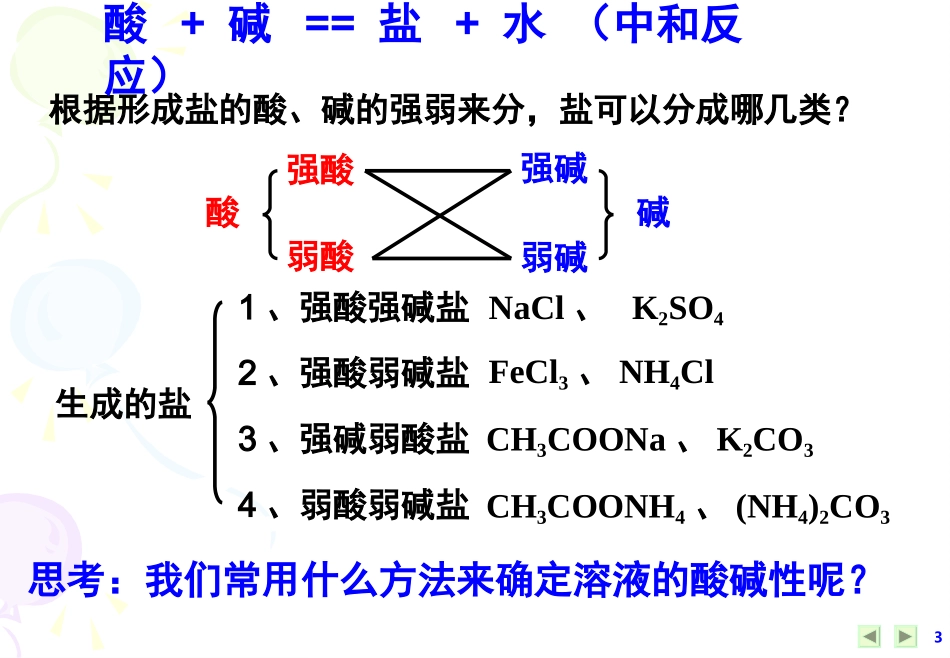
3根据形成盐的酸、碱的强弱来分,盐可以分成哪几类
酸+碱==盐+水(中和反应)酸强酸弱酸弱碱强碱碱生成的盐1、强酸强碱盐2、强酸弱碱盐3、强碱弱酸盐4、弱酸弱碱盐NaCl、K2SO4FeCl3、NH4ClCH3COONH4、(NH4)2CO3CH3COONa、K2CO3思考:我们常用什么方法来确定溶液的酸碱性呢
4盐溶液NaClNa2CO3NaHCO3NH4ClKNO3CH3COONa(NH4)2SO4酸碱性pH值盐的类型实验内容:分别测以下7种盐溶液的pH值,确定它们的酸碱性
用洁净的玻璃棒蘸取待测液滴于试纸中央,待变色后,与标准比色卡对比
4中性酸性碱性中性碱性碱性酸性=7>7<7=7>7>7<7强酸强碱盐强碱弱酸盐强碱弱酸盐强酸弱碱盐强酸强碱盐强碱弱酸盐强酸弱碱盐一、探究盐溶液的酸碱性的规律5二、盐溶液呈现不同酸碱性的原因H2OH++OH–纯水中:当分别加入NaCl、NH4Cl、CH3COONa形成溶液后,请思考:(1)相关的电离方程式
(2)盐溶液中存在哪些粒子
(3)哪些粒子间可能结合(生成弱电解质)
(4)对水的电离平衡有何影响
(5)相关的化学方程式
分析后,填写书P55表格6⑴电离方程式⑵c(H+)和c(OH–)相对大小⑶盐溶液的酸碱性⑷盐溶液中的粒子⑸有无弱电解质生成⑹相关化学方程式【探究1】往水中加NH4Cl形成溶液
H2OH++OH–NH4ClCl–+NH4++有(促进水的电离)NH3·H2Oc(H+)c(OH–)>酸性Cl–、NH4