第1节构成物质的基本微粒(第三课时)教学目标(1)知道原子是有原子核和核外电子构成的
(2)知道原子本身及内部各种微粒的带电情况和质量关系
(3)了解原子的实际质量和相对质量,能根据相对原子质量求算相对分子质量
教学重点和难点重点:原子的构成难点:相对原子质量的计算教学过程:一、自主尝试1.科学家研究发现
原子是由带的原子核和带的核外电子构成的
两者所带电量,电性,因而原子呈
2.原子核一般是由和两种微粒构成的,其中不带电,每个带一个单位的电荷
3.原子中:核内质子数______核外电子数核电荷数(选填“大于”、“小于”或“等于”)二、互动探究【阅读】书P68【问题研究】讨论“联想与启示”中的实验现象,得到什么启示
(1);(2);(3)
【阅读】书P69小结:1
原子构成:2
电性:质子带电、电子带电、中子电,且质子和电子所带电荷电量、电性,所以整个原子电
数量关系:数=数=数相对原子质量(Ar(某原子)):以作为基准,其他原子的质量与这一基准的比;单位为
计算式:相对原子质量(Ar(某原子))==数值关系:相对原子质量==数+数相对分子质量(Mr):等于构成分子的的总和
【课堂练习】1
原子是由和构成的
两者所带得电量,电性
2.原子核一般是由和两种微粒构成的,其中不带电,每个带一个单位的电荷
原子中:核内质子数______核外电子数核电荷数(选填大于、小于或等于)4
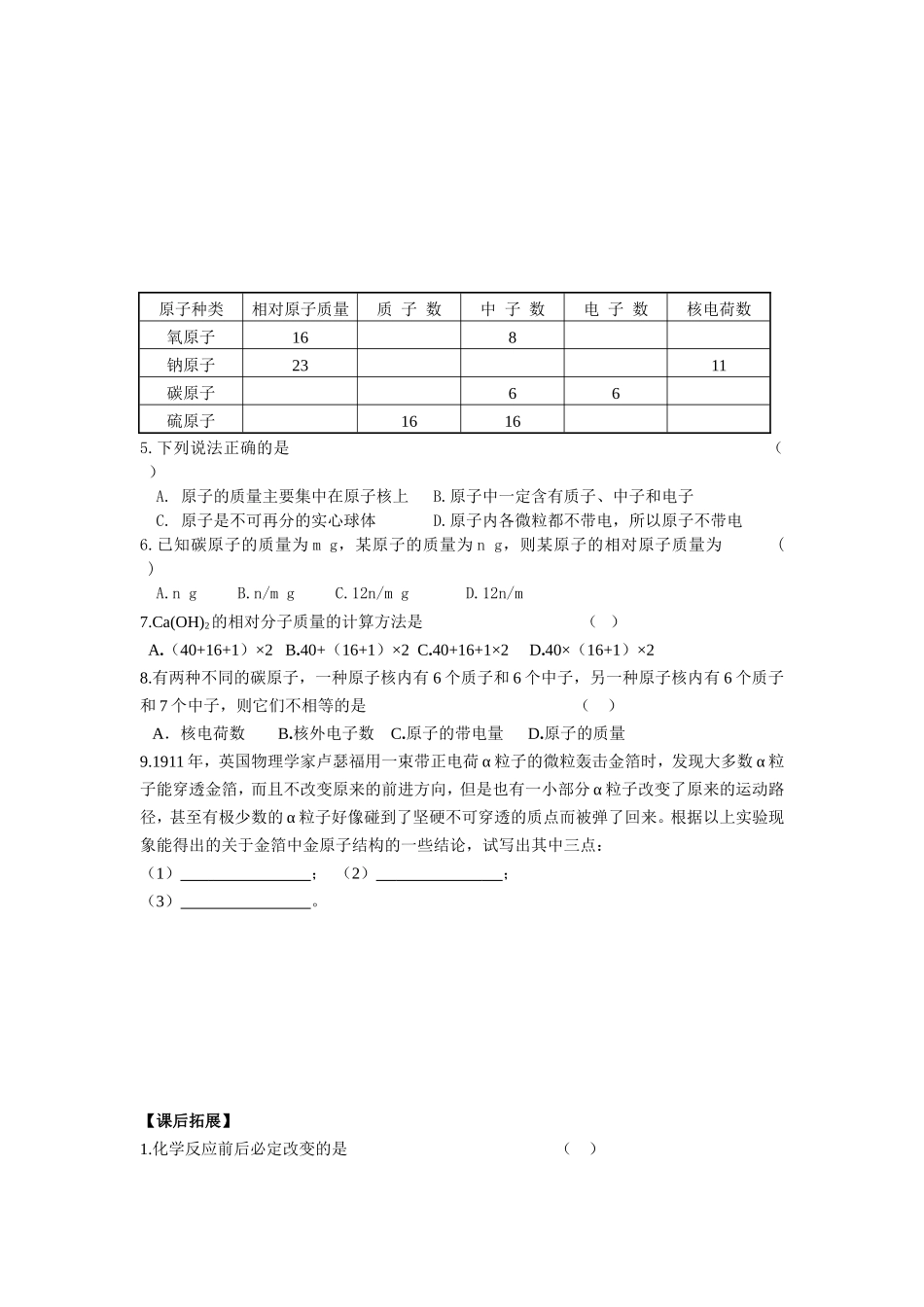
填写下表中的空白处:5
下列说法正确的是()A
原子的质量主要集中在原子核上B
原子中一定含有质子、中子和电子C
原子是不可再分的实心球体D
原子内各微粒都不带电,所以原子不带电6
已知碳原子的质量为mg,某原子的质量为ng,则某原子的相对原子质量为()A
12n/mgD
12n/m7
Ca(OH)2的相对分子质量的计算方法是()A
(40+16+1)×2B
40+(16+1)