化学反应原理:第四单元难溶电解质的沉淀溶解平衡省扬高中马玲玲2014年5月27日复习回顾1
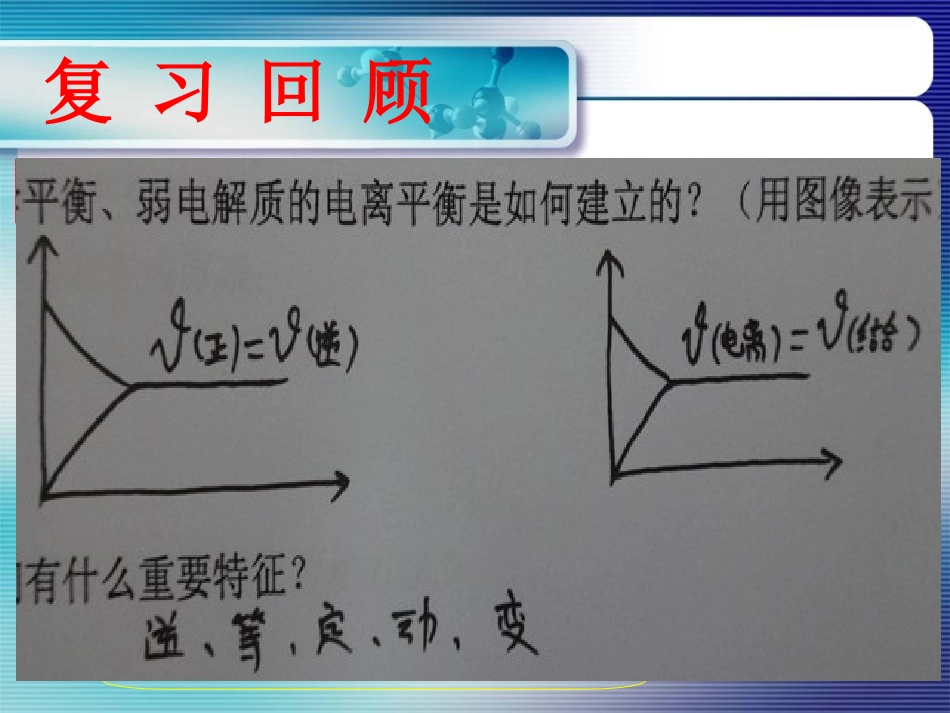
化学平衡、弱电解质的电离平衡是如何建立的
它们有什么重要特征
逆、等、定、动、变VVtt00VV((正正))VV((逆逆))VV((正正)=)=VV((逆逆))VVtt00弱电解质分子电离离子结合为弱电解质分子化学平衡状态电离平衡状态合作探究学习已知:PbI2难溶于水,AgI是黄色沉淀
问题1:将少量PbI2固体加入盛有一定量水的烧杯中,用玻璃棒充分搅拌,有什么现象
问题2:静置,取上层清液滴加AgNO3溶液,预计会有什么现象发生
(1)将少量PbI2固体加入盛有一定量水的50mL烧杯中,用玻璃棒充分搅拌,静置一段时间
(2)取上层清液2mL,加入试管中,逐滴加入AgNO3溶液,振荡,观察实验现象
探究分组实验产生黄色沉淀
PbI2Pb2++2I-+Ag+AgI合作探究学习问题1:画出沉淀溶解平衡的图像
问题2:沉淀溶解平衡的特点
问题3:影响沉淀平衡移动的因素
问题4:什么是沉淀溶解平衡
什么是溶度积
其表达式是什么
沉淀溶解平衡原理沉淀溶解平衡的特征动:等:定:变:动态平衡V溶解=V沉淀≠0外界条件一定,各粒子的浓度保持不变外界条件改变,沉淀溶解平衡发生移动沉淀溶解平衡沉淀溶解平衡原理影响沉淀溶解平衡的因素1
外因:难溶电解质本身的性质温度:浓度:温度升高,多数溶解平衡向溶解方向移动稀释:同离子效应:能反应的物质:向溶解方向移动加入相同的离子,向生成沉淀的方向移动反例:Ca(OH)2在有固态Mg(OH)2存在的饱和溶液中,存在着如下平衡:Mg(OH)2Mg2++2OH-
向该饱和溶液中分别加入水、升温、加固体MgCl2、加盐酸时,固体Mg(OH)2的质量有什么变化
加入与难溶电解质溶解所得的离子反应的物质,溶解平衡向溶解的方向移动沉淀溶解平衡原理定义:在一定的温度下