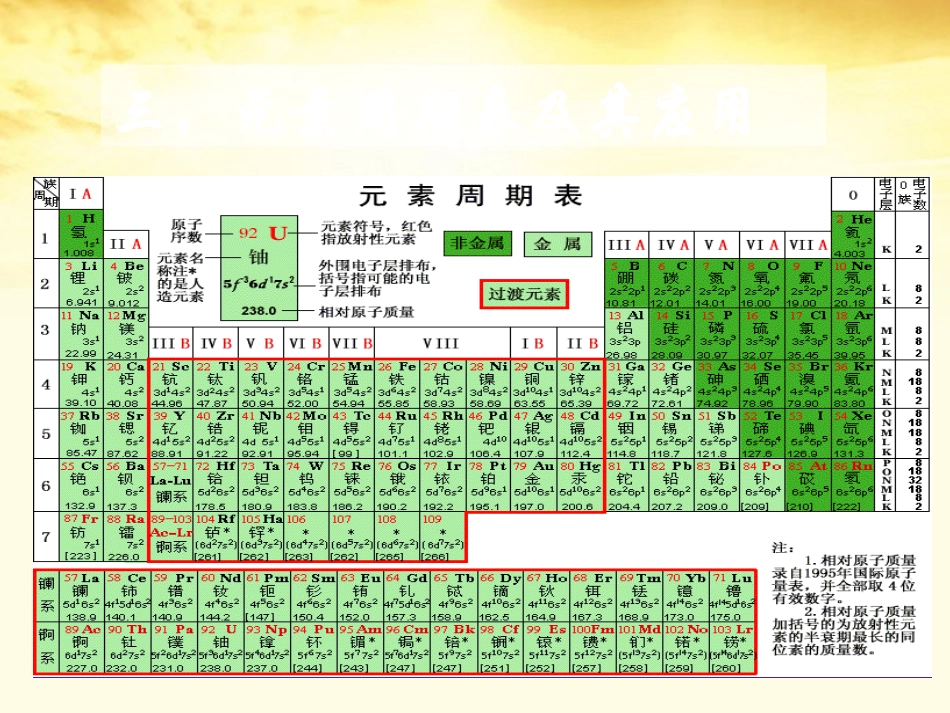
三、元素周期表及其应用P10元素周期表--门捷列夫元素周期律的具体表现形式1、编排原则:⑴按原子序数的递增顺序从左到右排列⑵将电子层数相同的元素排列成一个横行(周期)⑶把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行(族)仔细阅读研究图l一5所示的元素周期表,与同学交流讨论下列问题
1.在元素周期表中,每个横行称为周期
在元素周期表中共有多少个周期
每个周期各有多少种元素
在元素周期表中,每个纵行称为族
元素周期表中有哪些族
P8“交流与讨论”周期短周期长周期第1周期:2种元素第2周期:8种元素第3周期:8种元素第4周期:18种元素第5周期:18种元素第6周期:32种元素不完全周期第7周期:26种元素(预测有32种)(横向)2、周期表的结构:周期序数=电子层数族主族(A):副族(B):ⅠA,A,A,A,A,A,AⅡⅢⅣⅤⅥⅦ第VIII族:稀有气体元素主族序数=最外层电子数=最高化合价0族:共七个主族:长短周期共同组成ⅢB,B,B,B,BⅣⅤⅥⅦ;B,BⅠⅡ共七个副族:仅由长周期组成三个纵行,位于ⅦB与ⅠB中间(纵向)2、周期表的结构:•2.找出氮、硫、钠、铝、氖等元素在元素周期表中的位置(所在的周期和族),分析这些元素的原子核外电子层数、最外层电子数和元素所在的周期序数的关系
除氖元素外,其他各元素原子的最外层电子数与该元素所在的族序数有什么关系
思考:Cl在元素周期表中位置的描述
第七主族VII族VIIA族第III周期第三周期第3周期第三周期VIIA族元素在周期表中位置的描述7个周期分长短,3短3长1不全;18纵行16族,7主7副Ⅷ和0
镧系、锕系排下边
小结:最外层电子数原子半径化合价金属性(失电子能力)还原性非金属性(得电子能力)氧化性1→8逐渐增多逐渐减小逐渐减弱逐渐增强同周期元素即同一横行元素,电子层数相同随着核电荷数的递增逐渐升高同主族元素即同一纵行