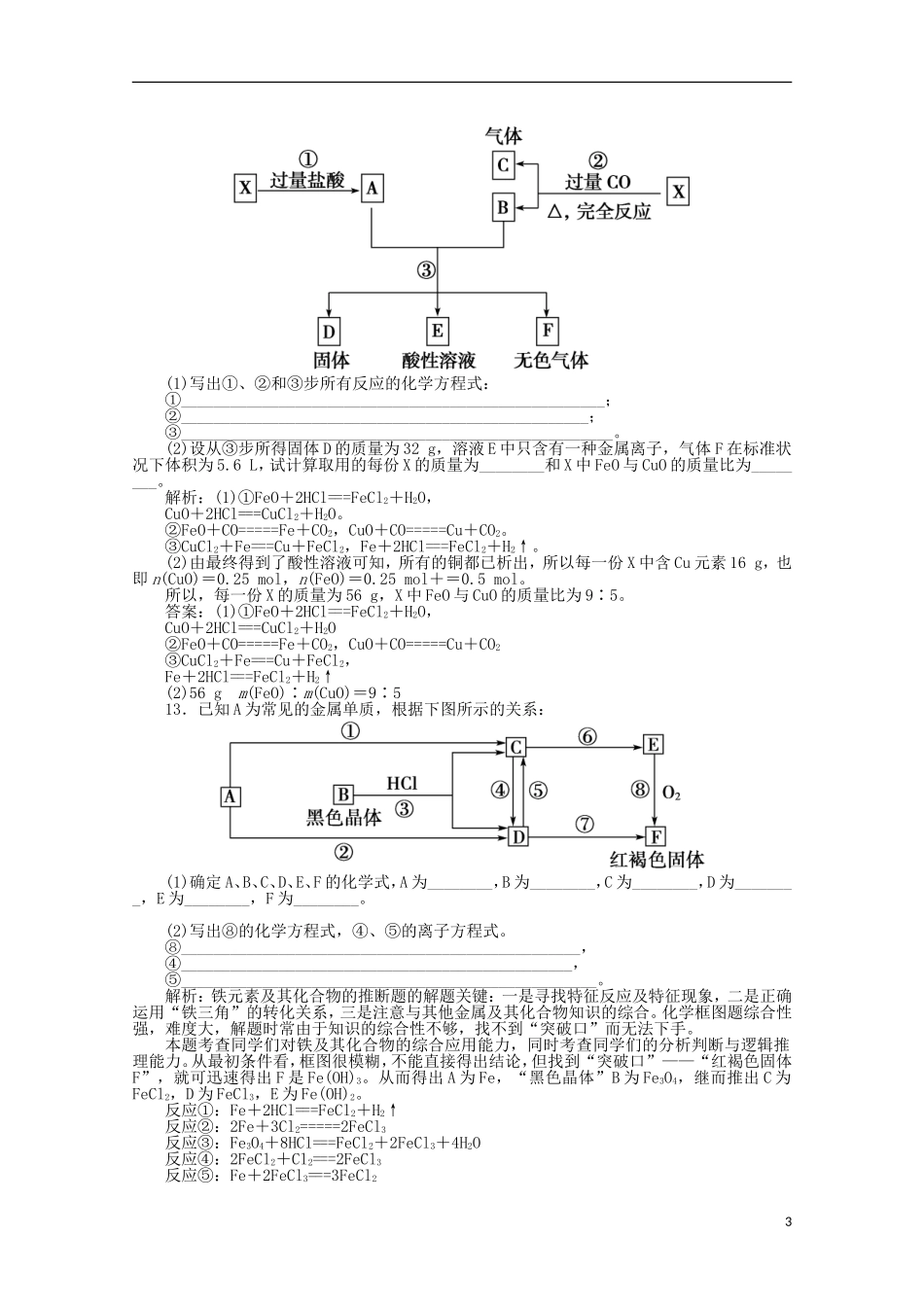
1.用一定量的铁与足量的稀硫酸及足量的CuO制单质铜,有人设计了以下两种方案:①Fe――→H2――→Cu②CuO――→CuSO4――→Cu若按实验原则进行操作,则两者制得单质铜的量为()A.一样多B.①多C.②多D.无法判断解析:选C
铁的量一定,转移的电子数一定
由于氢气还原氧化铜的实验中开始需消耗氢气排净装置中的空气,实验结束后铜粉需在氢气氛围下冷却,所以能够用于还原氧化铜的氢气量较少,根据电子守恒原理可知,①制得铜较少
2.下列说法正确的是()A.铜的化学性质活泼,不宜用铜制作盛食品的器皿B.铜的导电能力不如铝C.由于Cu2+有氧化性,所以用CuSO4来配制农药D.因为Cu2+能使蛋白质变性,所以铜盐溶液有毒解析:选D
金属铜的化学性质比较稳定,所以使用铜器皿比较安全;铜属于重金属,铜盐有毒,因Cu2+会与蛋白质作用,使蛋白质变性
3.由FeO、Fe2O3、Fe3O4组成的混合物,测得其中铁元素与氧元素的质量之比为21∶8,则这种混合物中FeO、Fe2O3、Fe3O4的物质的量之比可能为()A.1∶2∶1B.1∶2∶3C.1∶3∶1D.1∶1∶3解析:选D
由铁元素与氧元素的质量之比为21∶8,求得铁元素与氧元素的物质的量之比为3∶4,所以Fe3O4的量多少不影响混合物中的铁元素与氧元素的比
Fe3O4可拆为FeO·Fe2O3,故只要FeO、Fe2O3物质的量之比为1∶1即可
4.(2010年泰安高一检测)将适量铁粉投入三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是()A.2∶3B.3∶2C.1∶2D.1∶1解析:选A
铁粉与三氯化铁溶液反应Fe+2Fe3+===3Fe2+,设溶液反应后Fe2+物质的量为3mol,则反应掉Fe3+为2mol,剩余Fe3+为3mol,所以为2∶3
采用特殊值法,往往会