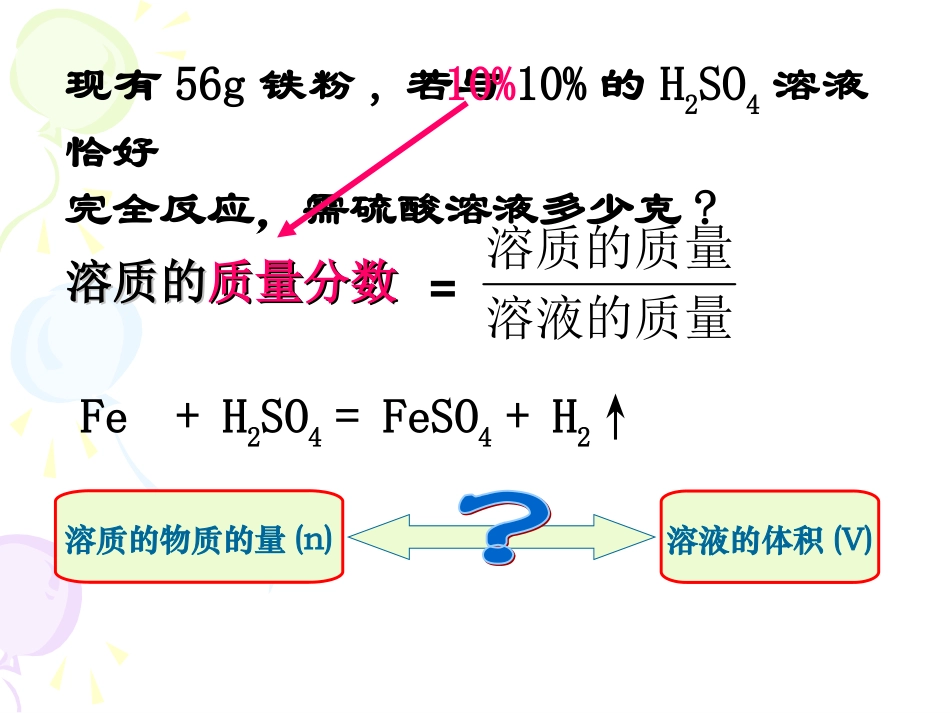
第一课时授课人董燕现有56g铁粉,若与10%的H2SO4溶液恰好完全反应,需硫酸溶液多少克
10%溶质的溶质的质量分数质量分数=溶液的质量溶质的质量Fe+H2SO4=FeSO4+H2↑溶质的物质的量(n)溶液的体积(V)m(质量)n(物质的量)V(气体体积)n(物质的量)迁移:MVm溶质的物质的量(n)溶液的体积(V)CCBB物质的量浓度物质的量浓度1、以单位体积溶液里所含溶质B的物质的量来表示溶液组成的物理量叫做溶质B的物质的量浓度
nB2、定义式CB=——V3、单位:mol/Lmol/m3简单应用简单应用nBCB=——V1、将0
5molNaCl固体溶于水中,配成250mL溶液,计算所得溶液中溶质的物质的量浓度
0mol/Lc(NaCl)=n(NaCl)V[NaCl(aq)]=0
5mol0.25L=2
0mol/L2、100mL1
0mol/L的KOH溶液中所含溶质的质量是
6gm(KOH)=c(KOH)×V[KOH(aq)]×M(KOH)=1
0mol/L×0
1L×56g/mol=5
6g3、将0
1molCaCl2溶于水配成200mL溶液,则所得溶液中CaCl2和Cl-物质的量浓度分别为多少
4、下列关于1
0mol·L-1的NaCl溶液的说法正确的是()A
溶液中含有1molNaClB
1L溶液中含有58
5gNaClC
1molNaCl溶于1L水中D
5gNaCl溶于941
5g水中B0
5mol/L;1mol/L注意注意1、溶液的体积不等于溶剂的体积;2、“溶质”的表示方法不是单一的;3、对于一定浓度的溶液,不论取用体积的多少,浓度都不变
•难电离的溶质-----以分子形式存在于溶液•完全电离的溶质----以离子形式存在于溶液(离子的数目要看物质的构成)CaCl2=Ca2++2Cl-容量瓶、烧杯、托盘天平、玻璃棒、胶头滴管实验仪器:100mL