金属的化学性质(第2课时)【学习目标】1
了解金属钠与水的反应,会解释钠与水反应的各种现象
了解铁与酸和水反应的实验原理、实验现象和生成产物
【学习过程】1
钠与水反应:实验步骤实验现象原因和结论用镊子取一小块钠置于滤纸上,吸干表面的煤油,用小刀切绿豆大的一粒,其余放回原瓶
在小烧杯中加一小半水,并将切下的钠粒投入小烧杯中,观察实验现象
反应结束后向烧杯中滴入1-2滴酚酞试剂,观察溶液的变化浮(钠浮在水面上)钠的密度小熔(钠熔化成一个闪亮的小球)钠与水反应放热,钠的熔点低游(钠球四处游动)钠与水反应产生的氢气不均匀,推动小球嘶(钠球发出嘶嘶的响声)钠与水反应产生的氢气冒出时发出声音红(钠球游过的地方酚酞溶液由无色变为红色)钠与水反应产生了碱性物质(1)按照不同的分类方法,钠与水的反应属于置换反应、离子反应、氧化还原反应、放热反应,Na是还原剂,H2O是还原剂,NaOH是氧化产物,H2是还原产物
2Na+2H2O=2Na++2OH―+H2↑温馨提示:①钠不能否保存在汽油或CCl4中
②钠与水反应过于剧烈,一般不用此反应制备H2
③金属钠失火不能用水或泡沫灭火器灭火,一般用砂土盖灭
(2)钠与酸溶液反应:钠与酸反应时先与酸中的H+反应,如果钠过量,钠把酸消耗尽之后,再与水反应
2Na+2HCl===2NaCl+H2↑温馨提示:Na与H2O和酸反应的实质都是与H+反应,而酸电离出的H+比水电离出的H+要大得多,故先与酸反应,现象与水反应相似,但更剧烈
(3)钠与盐溶液反应:钠与盐溶液反应时先与水反应,如果盐溶液中的溶质与氢氧化钠不反应,只发生钠与水的反应
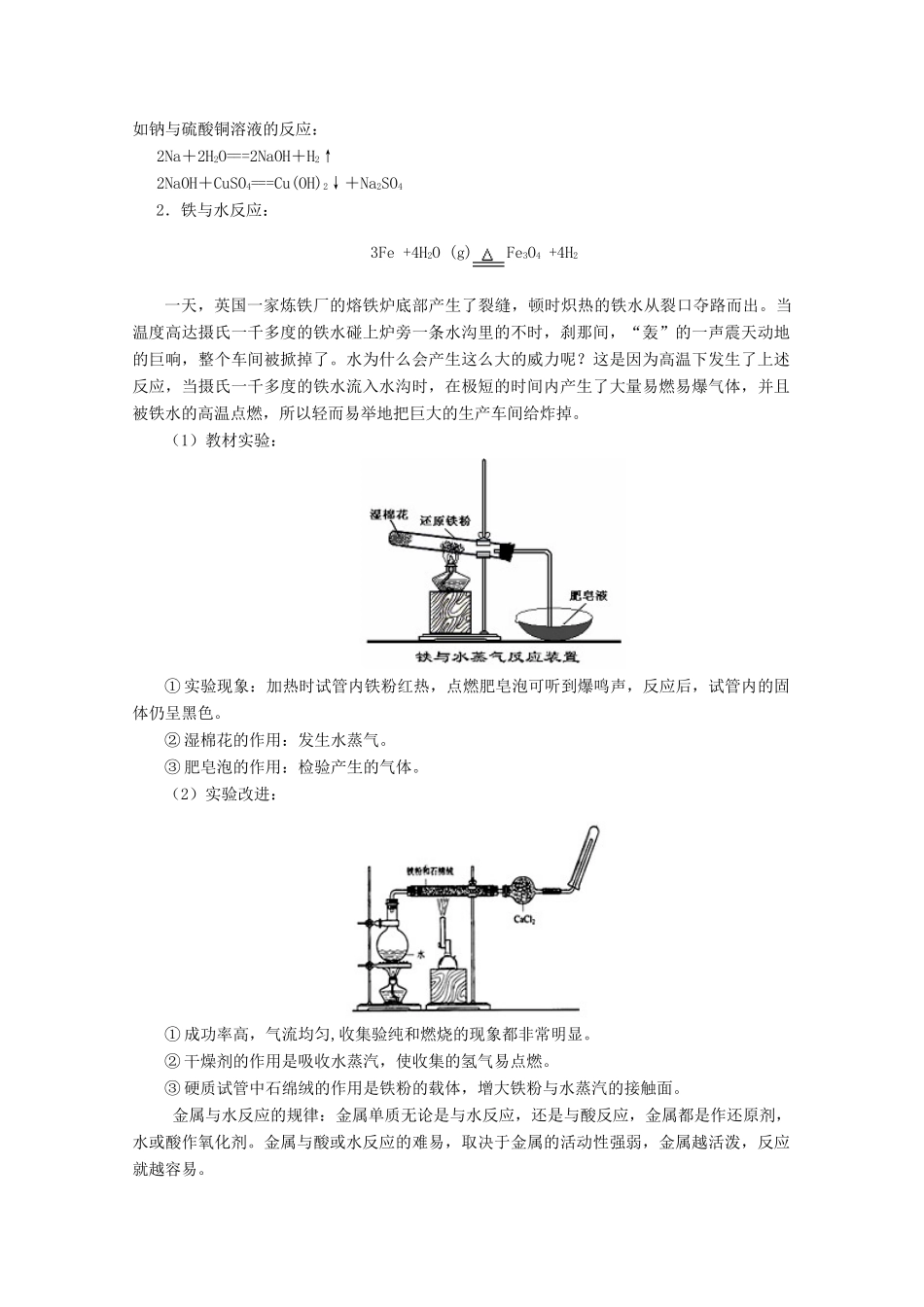
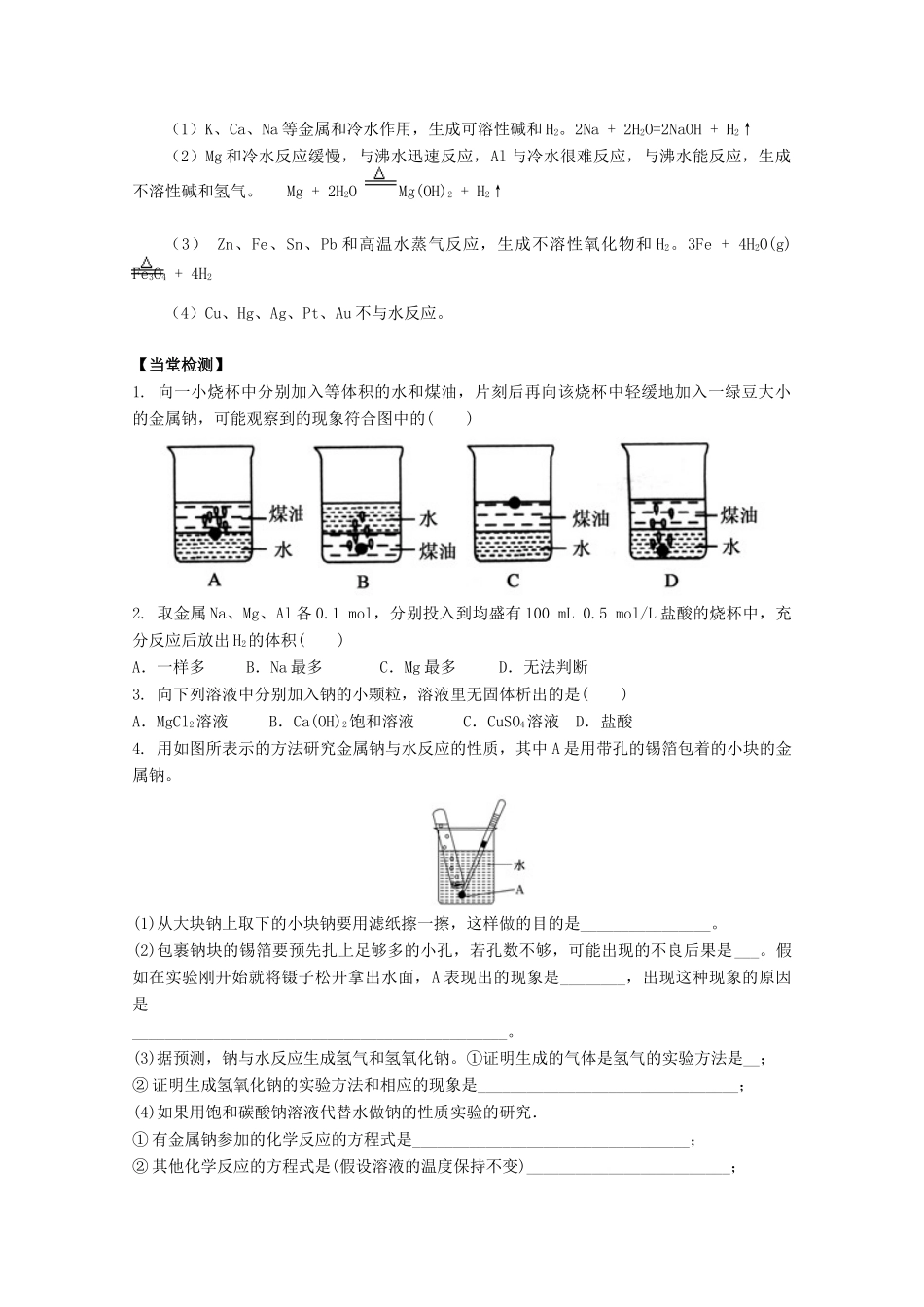
如果盐溶液中的溶质与氢氧化钠反应,则会发生两个反应,如钠与硫酸铜溶液的反应:2Na+2H2O===2NaOH+H2↑2NaOH+CuSO4===Cu(OH)2↓+Na2SO42.铁与水反应:3Fe+4H2O(g)Fe3O4+