课时1铁的单质、氧化物和氢氧化物发展目标体系构建1
了解铁的存在、应用、认识、应用铁的化学史,增强文化自信,培养学生“社会责任与科学精神”的核心素养
能用氧化还原反应原理认识铁的化学性质,同时根据实验事实探究Fe与H2O(g)的反应,培养学生“实验探究与证据推理”的核心素养
通过物质的属类和实验探究铁的氧化物和氢氧化物的主要性质和Fe(OH)2的制备探究,培养学生“科学探究与宏观辨识”的核心素养
一、铁的单质1.铁元素的存在铁元素在地壳中的含量仅次于氧、硅和铝,居第四位,主要是以+2价和+3价化合物的形态存在于矿石中
2.铁的冶炼(1)铁是目前产量最大,使用最广泛的金属
春秋初年,我国已掌握冶铁技术
(2)工业炼铁的原理是用还原方法把铁从铁矿石中提炼出来
高炉炼铁是用CO还原铁矿石(如Fe2O3)的化学方程式为Fe2O3+3CO=====2Fe+3CO2
3.物理性质铁有延展性和导热性
铁能导电,但其导电性不如铜和铝
铁能被磁体吸引
4.铁的化学性质铁的化学性质比较活泼,有较强的还原性,主要化合价为+2价和+3价
(1)铁与非金属单质、酸、盐溶液的反应①铁与氯气反应的化学方程式:2Fe+3Cl2=====2FeCl3
②加热条件下,铁与弱氧化性的S单质反应的化学方程式:Fe+S=====FeS
③铁与盐酸(稀硫酸)反应的离子方程式:Fe+2H+===Fe2++H2↑
④铁与硫酸铜溶液反应的离子方程式:Fe+Cu2+===Fe2++Cu
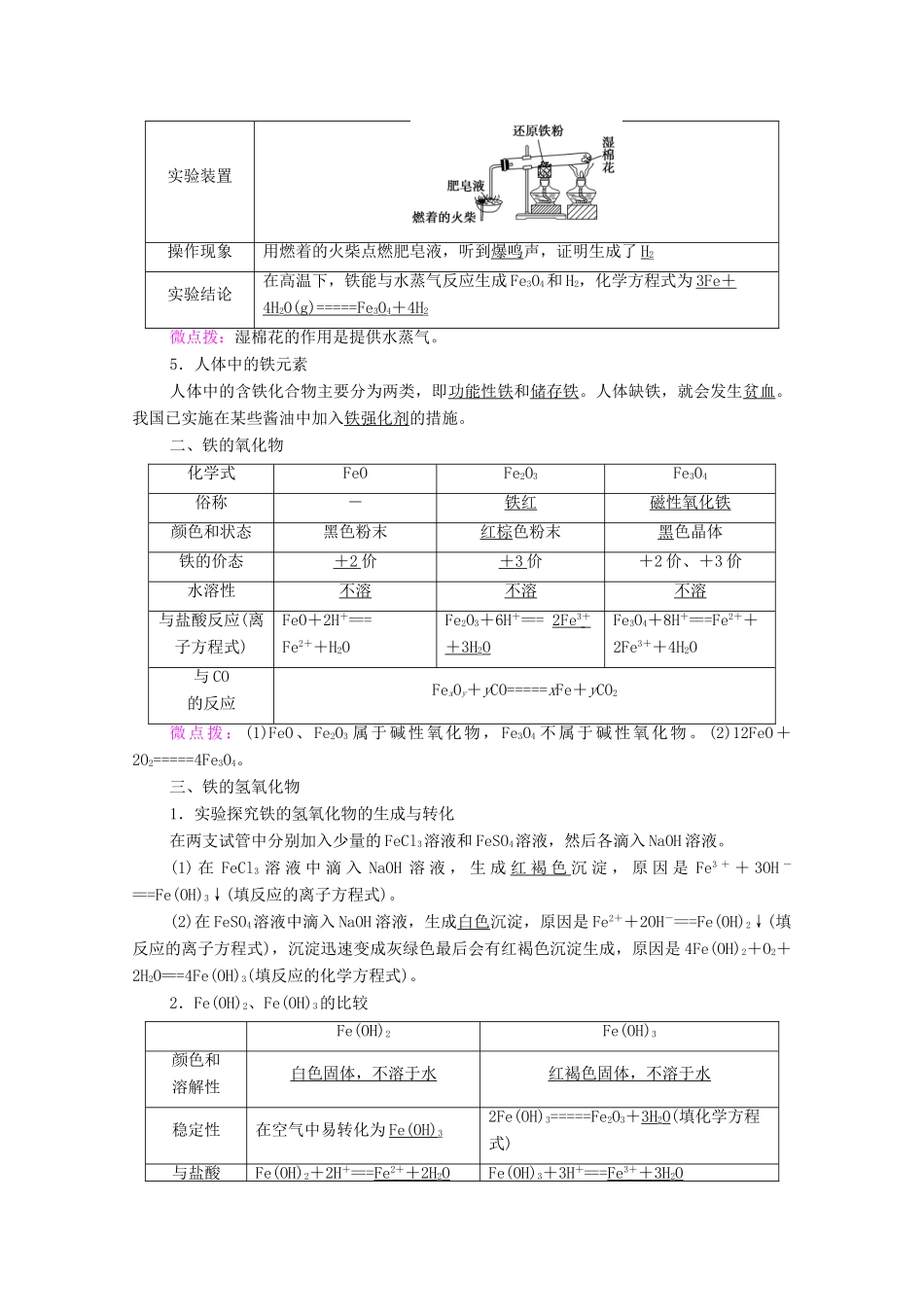
(2)实验探究铁粉与水蒸气的反应实验装置操作现象用燃着的火柴点燃肥皂液,听到爆鸣声,证明生成了H2实验结论在高温下,铁能与水蒸气反应生成Fe3O4和H2,化学方程式为3Fe+4H2O(g)=====Fe3O4+4H2微点拨:湿棉花的作用是提供水蒸气
5.人体中的铁元素人体中的含铁化合物主要分为两类,即功能性铁和储存铁
人体缺铁,就会发