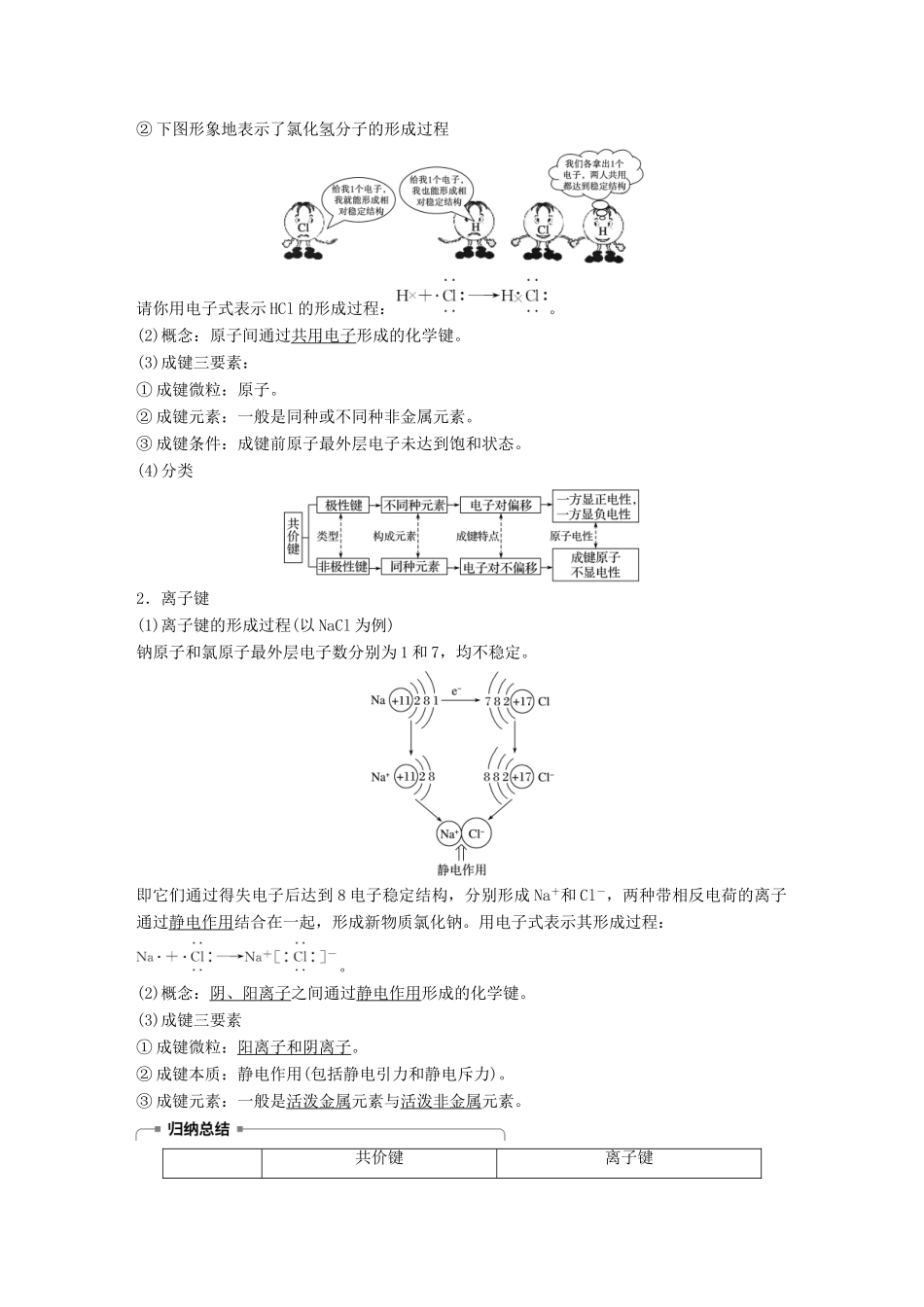
第1课时化学键及其类型一、化学键与物质变化1.化学键的概念相邻原子间的强相互作用称为化学键
2.用化学键的观点分析2H2O=====2H2↑+O2↑反应的过程:水分子断裂的是氢氧键,形成的是氢氢键和氧氧键
3.化学反应中物质变化的实质:旧化学键的断裂和新化学键的形成
(1)只有相邻的两个或多个原子间的强相互作用才能称为化学键
(2)判断一个变化过程中是否发生了化学反应,不仅要看有无旧化学键的断裂,而且还要看有无新化学键的形成
如果一个变化过程中只有旧键断裂而无新键形成,则该变化不是化学变化,如氯化氢溶于水,氯化氢分子中氢原子和氯原子间的化学键发生了断裂,但没有新化学键形成,故不属于化学变化
例1下列关于化学键的说法中正确的是()①相邻原子间的相互作用叫做化学键②化学键既存在于相邻原子间,又存在于相邻分子间③在水中氢、氧原子间均以化学键相结合④相邻原子之间强烈的相互吸引作用叫做化学键⑤化学键是指相邻原子间的强相互作用A.②③④B.③④⑤C.①②③D.只有⑤答案D解析①形成化学键的原子间的相互作用必须是强烈的,不强烈的相互作用不是化学键;②只有相邻原子间的强相互作用才是化学键,而相邻分子间的原子也可能相邻,但作用不强,不是化学键;③在水分子内,氧原子和氢原子之间形成化学键,但分子间的氧原子和氢原子间的相互作用很微弱,不是化学键;④化学键这种相互作用,是相邻原子间的原子核与电子之间的静电吸引、电子与电子之间的静电排斥、原子核与原子核之间的静电排斥达到平衡后的一种作用,所以化学键包括相互吸引和相互排斥;⑤正确
易错警示(1)形成化学键的原子必须相邻,但相邻的原子间不一定存在化学键
(2)“强相互作用”不能只理解为相互吸引
(3)并非所有的物质中都有化学键,如稀有气体是单原子分子,无化学键
例2下列变化不需要破坏化学键的是()A.加热氯化铵B.干冰升华C.水通电分解D.氯化氢溶于水答