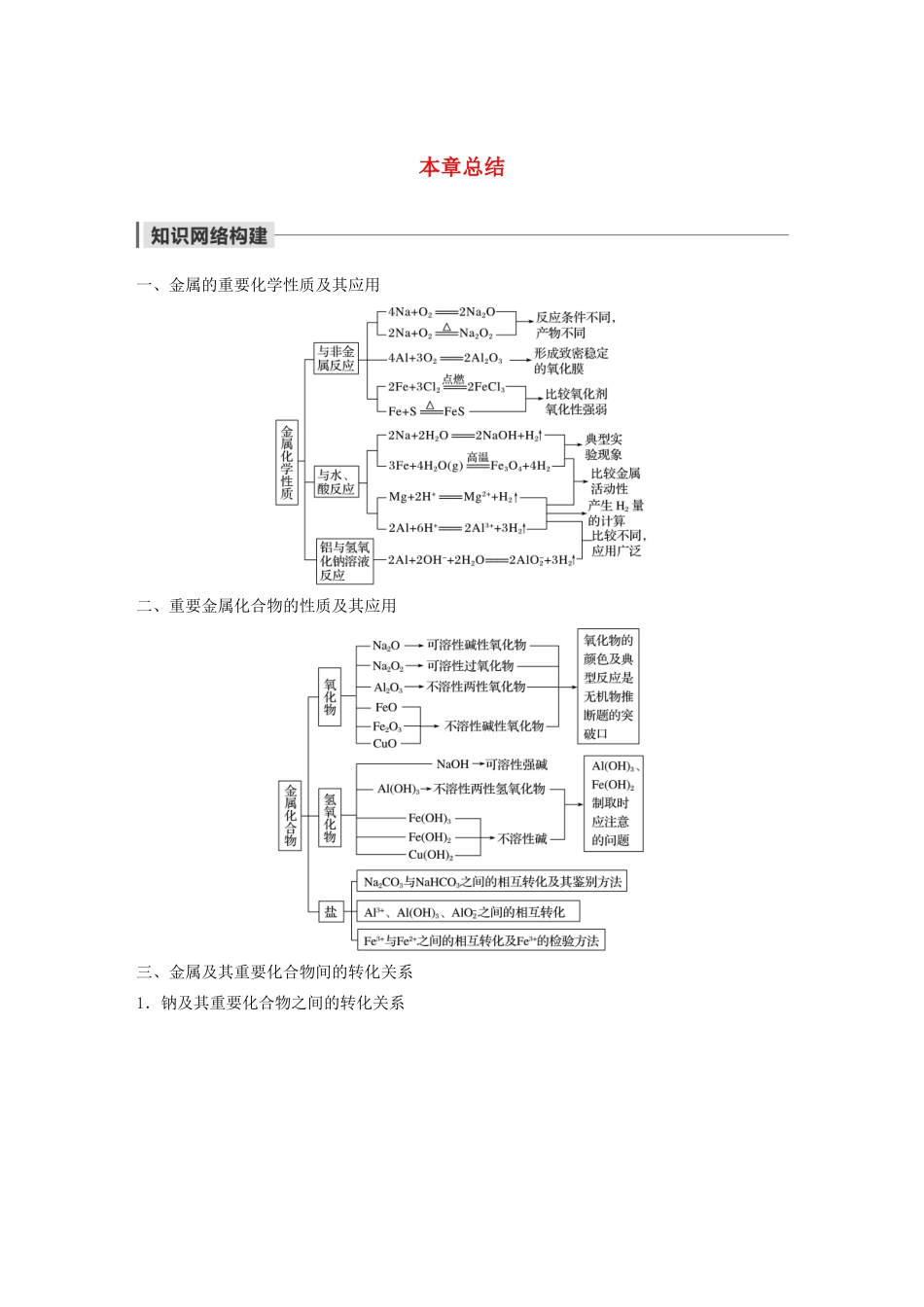
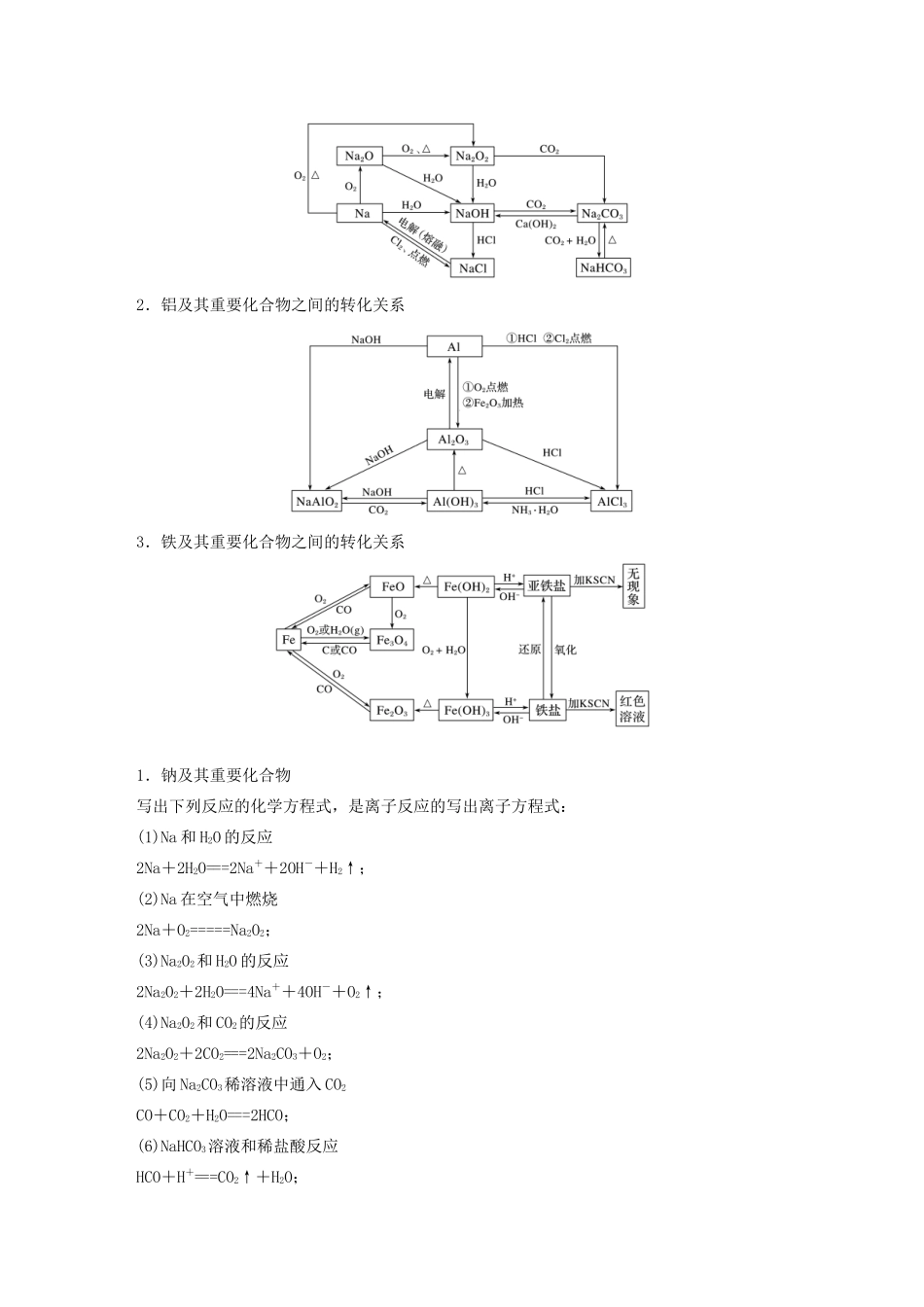
本章总结一、金属的重要化学性质及其应用二、重要金属化合物的性质及其应用三、金属及其重要化合物间的转化关系1.钠及其重要化合物之间的转化关系2.铝及其重要化合物之间的转化关系3.铁及其重要化合物之间的转化关系1.钠及其重要化合物写出下列反应的化学方程式,是离子反应的写出离子方程式:(1)Na和H2O的反应2Na+2H2O===2Na++2OH-+H2↑;(2)Na在空气中燃烧2Na+O2=====Na2O2;(3)Na2O2和H2O的反应2Na2O2+2H2O===4Na++4OH-+O2↑;(4)Na2O2和CO2的反应2Na2O2+2CO2===2Na2CO3+O2;(5)向Na2CO3稀溶液中通入CO2CO+CO2+H2O===2HCO;(6)NaHCO3溶液和稀盐酸反应HCO+H+===CO2↑+H2O;(7)NaHCO3溶液和NaOH溶液反应HCO+OH-===CO+H2O;(8)NaHCO3受热分解2NaHCO3=====Na2CO3+CO2↑+H2O
2.铝及其重要化合物写出下列反应的离子方程式:(1)Al与盐酸反应2Al+6H+===2Al3++3H2↑;(2)Al和NaOH溶液的反应2Al+2OH-+2H2O===2AlO+3H2↑;(3)Al(OH)3和NaOH溶液的反应Al(OH)3+OH-===AlO+2H2O;(4)Al(OH)3和盐酸的反应Al(OH)3+3H+===Al3++3H2O;(5)Al2O3和NaOH的反应Al2O3+2OH-===2AlO+H2O;(6)Al2O3和盐酸的反应Al2O3+6H+===2Al3++3H2O;(7)AlCl3溶液与氨水反应Al3++3NH3·H2O===Al(OH)3↓+3NH
3.铁及其重要化合物写出下列反应的化学方程式,是离子反应的写出离子方程式:(1)Fe在Cl2中燃烧2Fe+3Cl2=====2Fe