课题:第一节:无机非金属材料的主角-硅课时:第一课时学习目标:1
掌握二氧化硅的物理和化学性质;2
掌握硅酸的物理和化学性质3
提高实验设计能力难点重点:SiO2的结构和SiO2和硅酸的性质学习任务:一.硅元素的存在二.硅单质1.种类及结构:单质硅分为晶体硅和无定形两类,晶体硅的结构与金刚石类似
2.性质(1)物理性质:色、态光泽熔点硬度质地导电性灰黑色固体金属光泽高大脆半导体(2)化学性质:1
Si+O2高温SiO2,Si+2Cl2高温SiCl4,Si+C高温SiC,2F2+Si===SiF42特性:Si+4HF===SiF4↑+2H2↑,Si+2NaOH+H2O===Na2SiO3+2H2↑
3.用途:(1)半导体材料,如硅芯片,半导体晶体硅;(2)新型能源,如光电池等
三.二氧化硅1
存在:SiO2存在形态有结晶形和无定形两大类,统称硅石
石英、水晶、玛瑙、沙子、光导纤维的主要成分均是SiO22.结构:SiO2晶体是四面体空间网状结构3.物理性质:SiO2的熔点高,硬度大,不溶于水4
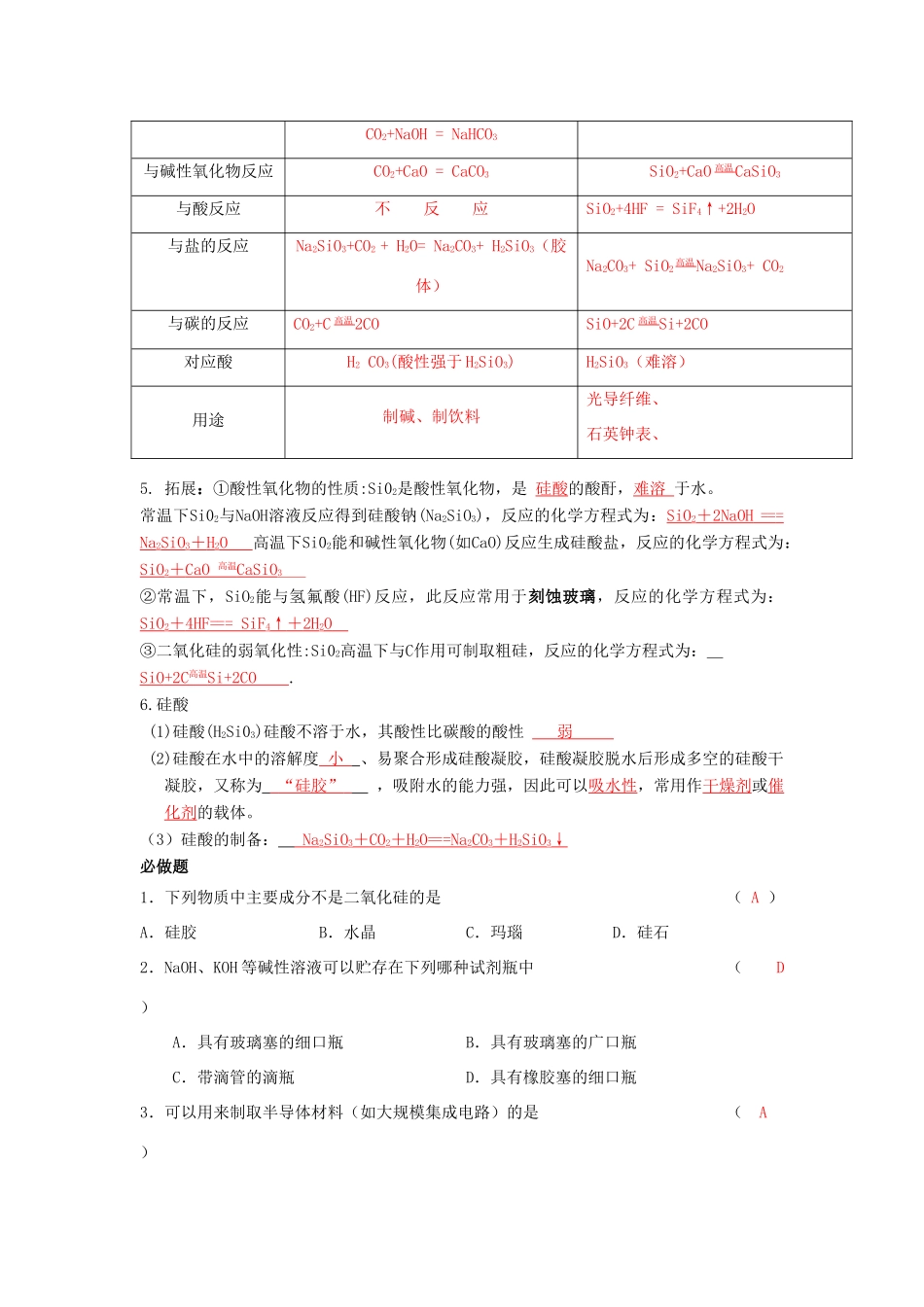
SiO2与CO2化学性质的比较性质二氧化碳(CO2)二氧化硅(SiO2)与水反应CO2+H2O=H2CO3不反应与碱反应CO2+2NaOH=Na2CO3+H2OSiO2+2NaOH=Na2SiO3+H2OCO2+NaOH=NaHCO3与碱性氧化物反应CO2+CaO=CaCO3SiO2+CaO高温CaSiO3与酸反应不反应SiO2+4HF=SiF4↑+2H2O与盐的反应Na2SiO3+CO2+H2O=Na2CO3+H2SiO3(胶体)Na2CO3+SiO2高温Na2SiO3+CO2与碳的反应CO2+C高温2COSiO+2C高温Si+2CO对应酸H2CO3(酸性强于H2SiO3)H2SiO3(难溶)用途制碱、制饮料光导纤维、石英钟表、5
拓展:①酸性氧化物的性质:Si02是酸性氧化物,是硅酸