高三化学晶体类型与性质人教版【同步教育信息】一
本周教学内容:晶体类型与性质二
重点、难点:1
使学生了解离子晶体、分子晶体和原子晶体的晶体结构模型及其性质的一般特点
使学生理解离子晶体、分子晶体和原子晶体的晶体类型与性质的关系3
使学生了解分子间作用力对物质物理性质的影响4
常识性介绍氢键及其物质物理性质的影响
具体内容:(一)晶体固体可以分为两种存在形式:晶体和非晶体
晶体的分布非常广泛,自然界的固体物质中,绝大多数是晶体
气体、液体和非晶体在一定条件下也可转变为晶体
晶体是经过结晶过程而形成的具有规则的几何外形的固体
晶体中原子或分子在空间按一定规律周期性重复的排列,从而使晶体内部各个部分的宏观性质是相同的,而且具有固定的熔点和规则的几何外形
(二)晶体结构1
几种晶体的结构、性质比较晶体类型离子晶体分子晶体原子晶体金属晶体定义阴阳离子间通过离子键形成的晶体分子间通过分子间作用力形成的晶体相邻原子间通过共价键结合而成的立体网状的晶体由金属阳离子和自由电子间相互作用形成的晶体构成粒子阴、阳离子分子原子金属离子、自由电子粒子间作用力离子键分子间力共价键金属键代表物NaCl,NaOH,MgSO4干冰,I2,P4,H2O金刚石,SiC,晶体硅,SiO2镁、铁、金、钠物理性质硬度较大,熔点、沸点较高,多数易溶于水等极性溶剂;熔化或溶于水时能导电
硬度小,熔点、沸点低;相似相溶;熔化时不导电,其水溶液可导电
硬度大,熔点、沸点高;难溶解;有的能导电,如晶体硅,但金刚石不导电
硬度差异较大,熔点、沸点差异较大,难溶于水(钠、钙等与水反应);晶体导电,熔化时也导电决定熔点、沸点高主要因素离子键强弱分子间作用力大小共价键强弱金属键强弱2
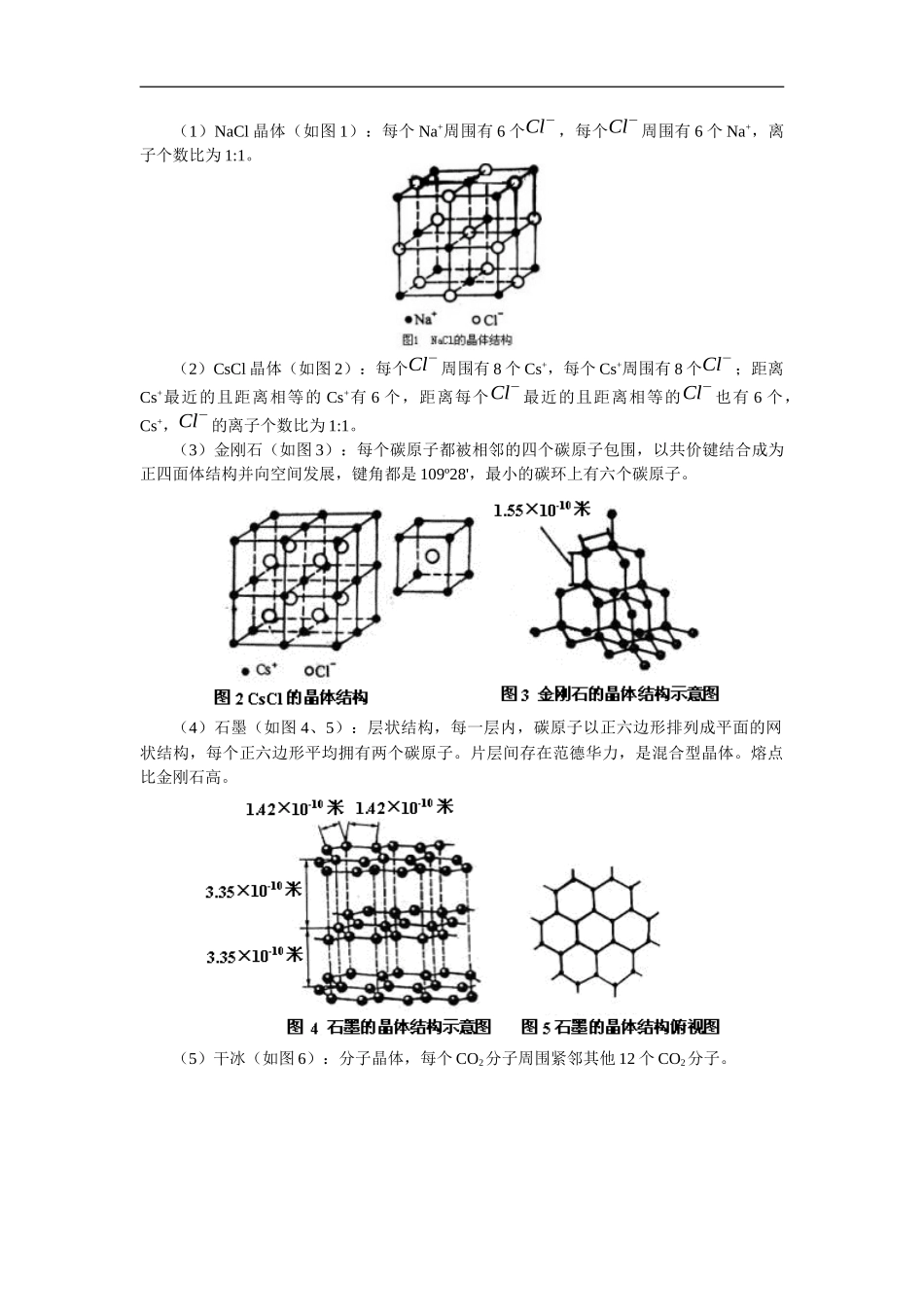
几种典型的晶体结构:(1)NaCl晶体(如图1):每个Na+周围有6个Cl−,每个Cl−周围有6个Na+,离子个数比为1:1
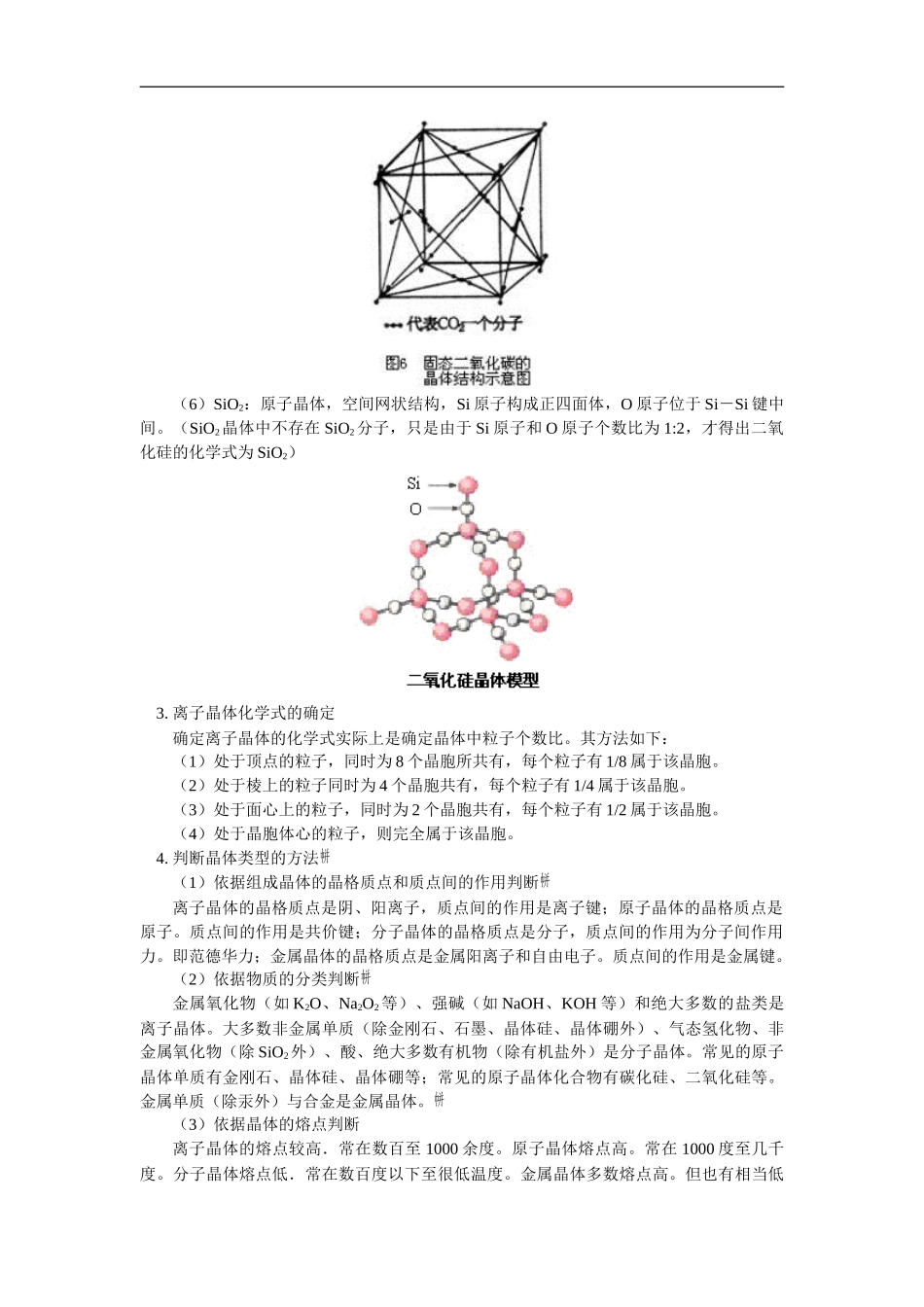
(2)CsCl晶