问题1:怎样理解元素周期律
1.元素周期律的概念:元素的性质随着的递增呈现周期性变化
2.元素周期律的实质:元素性质的周期性变化是元素原子的呈现周期性变化的必然结果
知识点1元素周期律原子序数核外电子排布尤其是最外层电子排布第二节元素周期律(表)思维延伸知识点2元素周期表问题2:元素周期表中包含哪些内容
3.元素周期表的结构元素周期表:4.原子结构与元素周期表的关系(1)核内=原子序数(2)周期序数=数(3)主族序数=数=数=数质子数电子层最外层电子最高正化合价8-|负价|问题3:怎样利用元素周期表
5.元素周期表中位置与元素性质的关系性质同周期(从左到右)同主族(从上到下)①金属性增强②非金属性增强③单质还原性增强④单质氧化性增强减弱减弱减弱减弱⑤最高价氧化物对应水化物的酸碱性碱性酸性碱性酸性⑥非金属形成气态氢化物的难易程度难→易易→难⑦气态氢化物的稳定性不稳定→稳定稳定→不稳定减弱增强增强减弱6
周期表在生产中的某些应用(1)农药多数是含元素的化合物
(2)半导体材料都是由周期表里的元素组成的,如Ge、Si等
(3)元素对许多化学反应都有良好的催化性能
(4)在元素周期表里从ⅢB到ⅡB的过渡元素,如钛、钨、铬等具有耐高温、耐腐蚀的特点
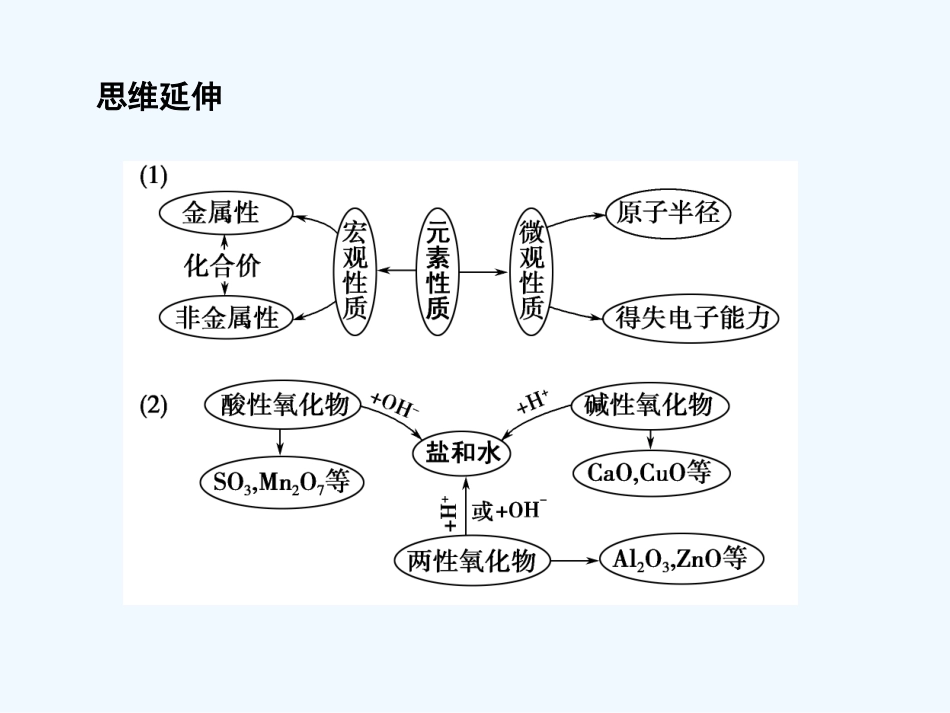
右上角(F、Cl、S、P)等分界线附近过渡金属思维延伸“位—构—性”之间的关系考点1元素金属性与非金属的强弱比较1.根据原子结构2.根据元素在周期表中的位置来判断(见知识点2)3.根据实验(1)金属性强弱比较①与水或酸反应置换氢的难易:越易者金属性越强
②最高价氧化物对应水化物的碱性强弱:碱性越强者金属性越强
③根据金属活动性顺序表:排在前面的金属性较强
④由电化学原理:一般情况下,不同金属和稀H2SO4形成原电池时,作负极的金属活泼
在电解池中的惰性电极上,先析出的金属金属性弱
⑤与盐溶液的置换反应:A置换出B,则A金属性强