(一)回顾(一)回顾&&思考思考(1)什么是分子、原子
(2)运用分子和原子的观点解释电解水这一化学变化
说明什么结论
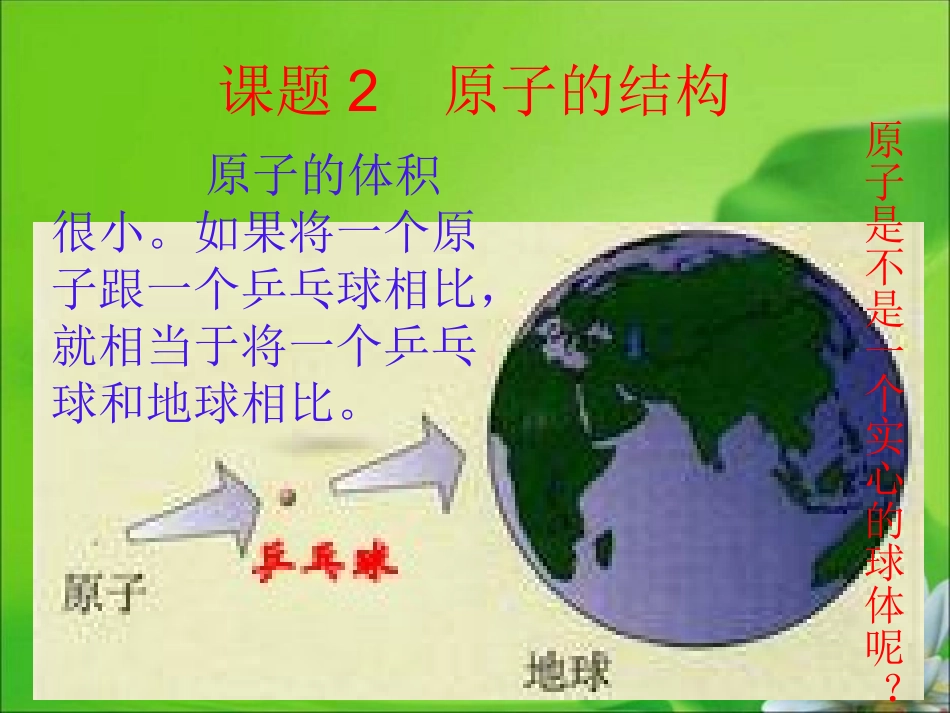
课题2原子的结构原子的体积很小
如果将一个原子跟一个乒乓球相比,就相当于将一个乒乓球和地球相比
原子是不是一个实心的球体呢
议一议1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带两个单位正电荷的氦原子)轰击金箔时,发现大多数α粒子能穿透金箔,而且不改变原来的运动方向,但是也有一小部分α粒子改变了原来的运动路径,甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来(如右图)
那么为什么有的α粒子可以穿透金箔,有的不行
你能解释其中的道理么
观察原子构成的示意图,你能得到什么信息
原子的构成一原子的构成原子原子核(+)核外电子(-)质子(+)中子(不带电)为什么原子对外不显电性呢
原子核内质子与核外电子所带的电性相反但电量相等,所以整个原子不显电性(p53)一个质子带一个单位正电荷一个电子带一个单位负电荷中子不带电原子种类原子种类质子数质子数(+)(+)中子数中子数(不带电)(不带电)核外电子数核外电子数(-)(-)氢氢110011碳碳666666氧氧888888钠钠111112121111磷磷151516161515铁铁262630302626氯氯171718181717这个表格反映出原子构成的哪些信息1、原子的构成:构成原子的粒子一般是质子、中子、电子(氢原子例外)(有一种氢原子中只有一个质子和一个核外电子,没有中子,即并不是所有原子里都有中子
在原子中,核电荷数=质子数=电子数3
质子数和中子数不一定相等,但很接近4
原子的种类不同,其质子数也不相同有一种原子的核电荷数为49,中子数为66,则这种原子的质子数和核外电子数分别为()A4966B6649C6666D4949核电荷数=质子数=核外电子数原子核(蚂蚁)原子