氨硝酸硫酸1
氮的存在一、氨气2
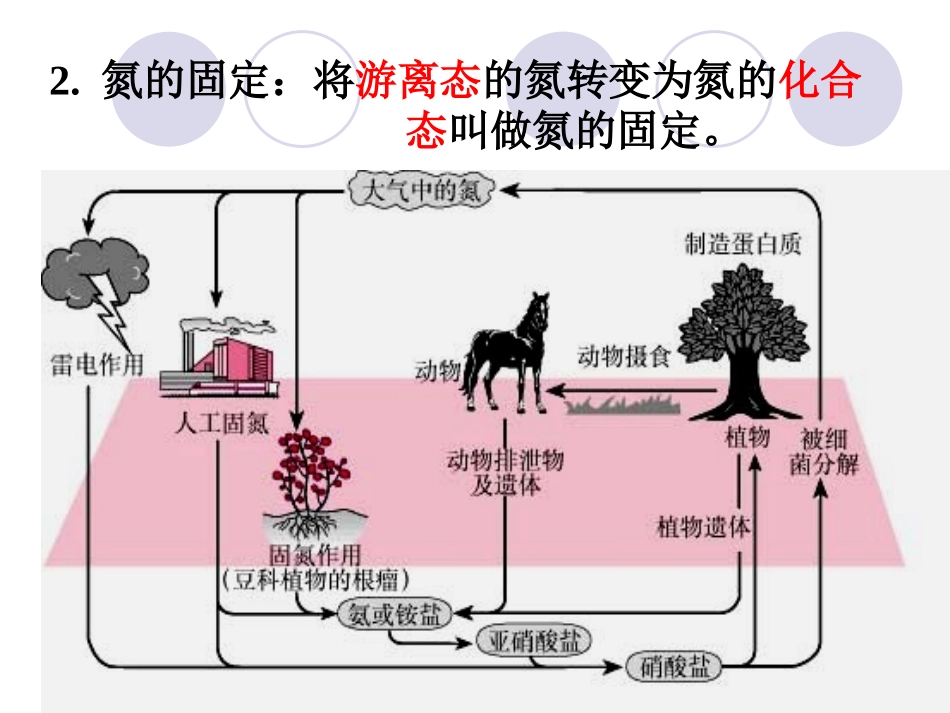
氮的固定:将游离态的氮转变为氮的化合态叫做氮的固定
(3)人工固氮:N2+3H22NH3高温、高压催化剂(2)自然固氮:N2+O22NO放电或高温(1)生物固氮:N2NH4+//NO3-根瘤菌哈伯(1868~1934)德国物理化学家,是合成氨法的发明者
因发明用氮气和氢气直接合成氨的方法,获1918年诺贝尔化学奖氨气(1)
氨气的物理性质密度:比空气小熔沸点:低,易液化(液氨)溶解性:极易溶于水(1700)∶色态:没有颜色、具有刺激性气味的气体(2)
氨的化学性质①氨与水反应----喷泉实验[现象]:形成红色的喷泉极易溶于水(1700)∶[原因]:NH3与水反应后有碱性物质生成
[结论]:(氨水显弱碱性,一水合氨是电解质,氨气不是电解质)NH3+H2ONH3·H2ONH4++OH-既能使无色的酚酞溶液变成________,又能使湿润的红色的石蕊试纸________
红色变蓝1.若用烧瓶收集满CO2,滴管(及烧杯中)中吸入下列何种液体时能形成喷泉
A、H2OB、稀硫酸C、NaCl溶液D、NaOH2、液氨和氨水的比较:液氨氨水形成氨气加压或降温后形成的液态物质氨气溶于水物质分类微粒种类混合物纯净物氨水中的分子有:H2O、NH3和NH3·H2O;氨水中的离子有:NH4+、OH-和少量H+NH3思考思考√2NH3+H2SO4==NH3+HNO3==[探索实验]将蘸有浓氨水的玻璃棒和蘸有浓盐酸的玻璃棒靠近,现象是NH3+HCl==NH4Cl②NH3与酸反应生成铵盐思考:是否所有的酸与NH3反应都有白烟
结论:________________________________(NH4)2SO4NH4NO3烟:固体小颗粒挥发性的酸遇到NH3会有白烟产生大量白烟③氨的还原性----氨的催化氧化4NH3+5O24NO+6H2O△催化剂硝酸的制取过程N2NH3N