基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习第一节化学能与热能(第二课时)基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习【温故而知新】请学生解释化学反应中产生能量变化的原因
1、从化学键角度2、从物质储存能量角度基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习1.化学反应中能量变化的原因——微观角度(1)化学反应的实质原子的重新组合,即反应物中旧化学键的和生成物中新化学键的过程
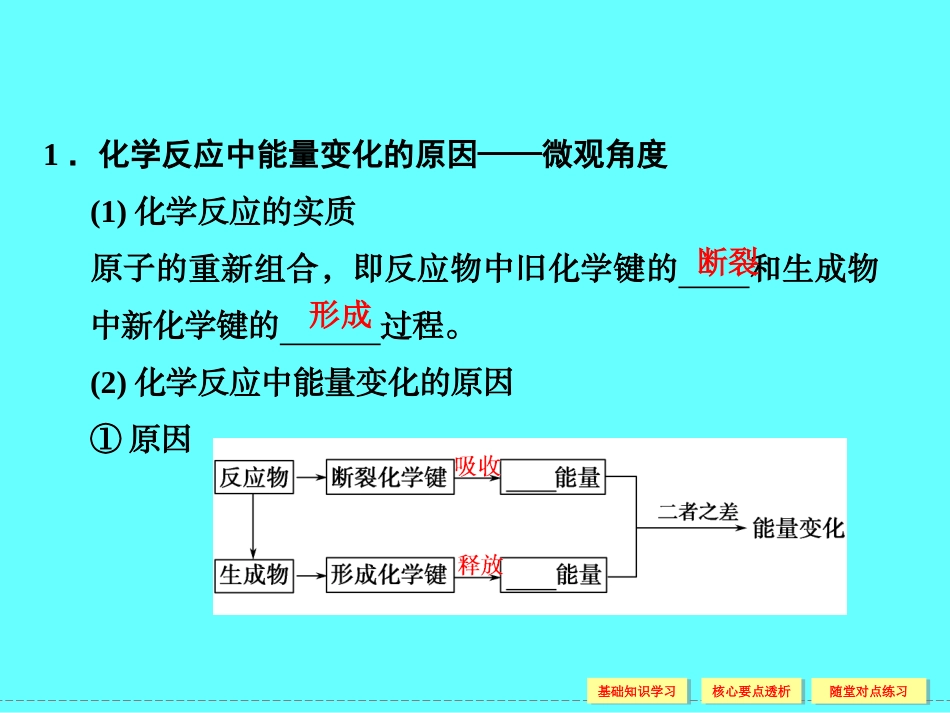
(2)化学反应中能量变化的原因①原因断裂形成基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习2.化学反应中能量变化的决定因素——宏观角度结论:化学反应中的能量变化决定于的相对大小
反应物的总能量与生成物的总能量基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习二、化学能与热能的相互转化1
两条基本的自然定律总质量总能量基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习2
化学能与热能的相互转化(1)吸热反应和放热反应
①吸热反应:_____热量的化学反应
②放热反应:_____热量的化学反应
基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习现象结论分组实验1:盐酸与铝片的反应分组实验2:Ba(OH)2·8H2O与NH4Cl的反应现象结论反应放出热量
反应放出热量
有气泡放出,温度升高
有气泡放出,温度升高
有刺激性气味,烧杯底部有刺激性气味,烧杯底部很冷,烧杯下面的玻璃片很冷,烧杯下面的玻璃片被冻在一起
反应吸收热量
反应吸收热量
基础知识学习基础知识学习核心要点透析核心要点透析随堂对点练习随堂对点练习分组实验3:酸与碱的中和反应反应物及其用量酸HCl20mL1mol/LHNO320mL1mol/L碱NaOH20mL1m