元素周期律元素周期律第二节一
原子核外电子排布1
电子的能量电子在核外空间运动是分层的,在多电子原子中,在离核远近不同的区域运动的电子,它们具有的能量是不同的
能量低的电子在离核较近的区域运动,能量高的电子在离核较远的区域运动
即:离核越近能量越低;越远,能量越高
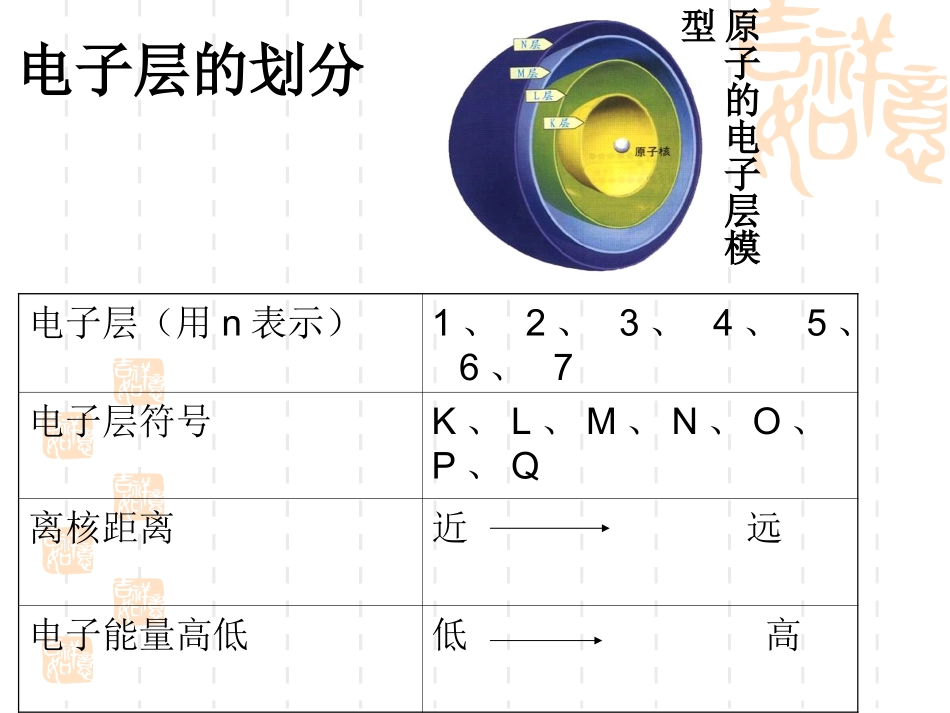
电子层根据电子能量的差别和通常运动区域的不同,可以认为,电子是在原子核外距核由近到远,能量则由低到高的不同电子层上分层排布的
通常能量最低,离核最近的电子层叫第一层,能量稍高,离核稍远的电子层叫做第二层,由里往外依次类推电子层的划分电子层(用n表示)1、2、3、4、5、6、7电子层符号K、L、M、N、O、P、Q离核距离近远电子能量高低低高原子的电子层模型归纳为:即核外电子总是尽先排布在的电子层里每层电子不能超过个最外层电子不能超过个(K层是最外层时不超过个)次外层电子不能超过个倒数第三层电子不能超过个
核外电子排布的一般规律能量最低2n2818322一低四不超注意:以上几条是相互联系的,不能孤立地理解其中的某一条
图1-1几种原子的核外电子排布示意图4
核外电排布的表示和应用创新教程第12面考点二5
元素的性质与元素的原子核外电子排布的关系(1)稀有气体的不活泼性:稀有气体元素的原子最外层有8个电子(氦是2个电子),处于稳定结构,因此化学性质稳定,一般不跟其他物质发生化学反应
(2)非金属性与金属性(一般规律):最外层电子数得失电子趋势元素的性质金属元素<4较易失金属性非金属元素>4较易得非金属性课堂练习1、某元素原子的K层电子数与M层电子数之和等于L层电子数,该元素是()A、SB、CC、OD、N2、画出第53号、88号元素的原子结构示意图A3
用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒,请真空:(1)A元素是------B元素是---------C元素是----------