1zxxkw学
网2从天然资源中提取有机物成分,首先得到的是含有机物的粗品
在工厂生产、实验室合成的有机化合物也不可能直接得到纯净物,得到的往往是混有未参加反应的原料,或反应副产物等的粗品
因此,必须经过分离、提纯才能得到纯品
如果要鉴定和研究未知有机物的结构与性质,必须得到更纯净的有机物
如何才能得到纯品呢
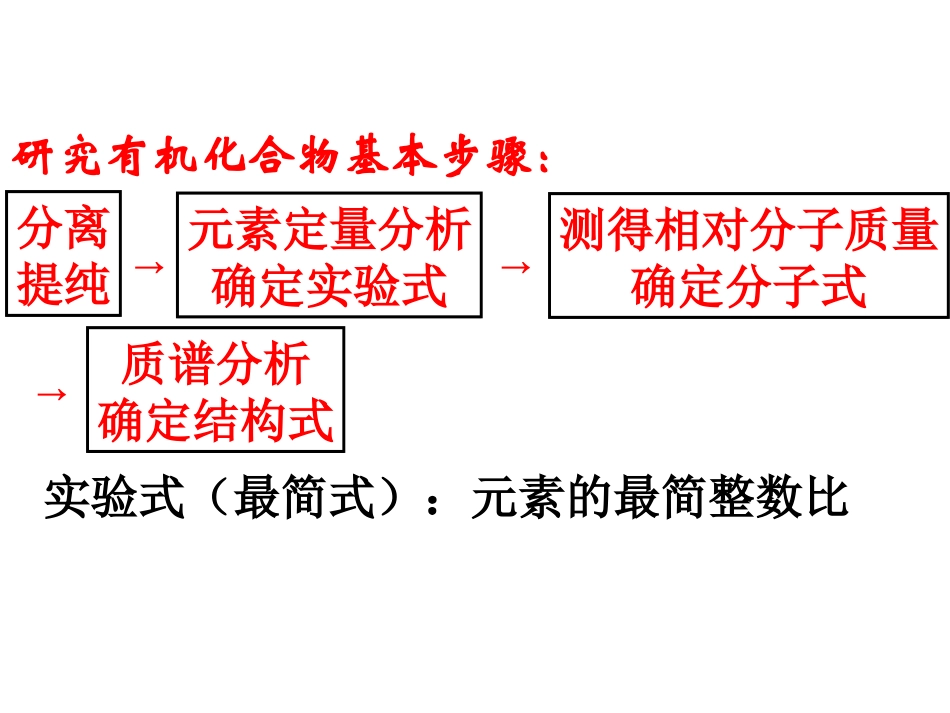
提出问题:3研究有机化合物基本步骤:分离提纯→元素定量分析确定实验式质谱分析确定结构式测得相对分子质量确定分子式→→实验式(最简式):元素的最简整数比zxxkw4eg:最简式为CH2O某有机物相对分子质量为60(1)写出有机物的分子式(2)若其官能团为-COOH,写出有机物的结构简式(3)若其官能团为-酯基,写出有机物的结构简式学
网51、常见的分离、提纯物质的方法有哪些
2、下列物质中的杂质(括号中是杂质)分别可以用什么方法除去
①酒精(水)②CO2(HCl)③KNO3(NaCl)④乙酸乙酯(乙醇)⑤甲烷(乙烯)⑥NaCl(泥沙)⑦溴水(水)思考与交流:6一、分离、提纯1、蒸馏利用液态有机物与杂质沸点不同(杂质为不挥发或难挥发,收集馏分)条件①有机物热稳定性较强②有机物与杂质沸点相差较大(一般约大于30)℃实验1-1:含有杂质的工业乙醇的蒸馏蒸馏(77-79℃的馏分)95
6%乙醇生石灰99
5%乙醇蒸馏zxxkw7注意事项:①温度计水银球置于蒸馏烧瓶支管口处②加入几粒沸石或碎瓷片③冷凝管应下端口进水上端口出水④烧瓶在石棉网上加热,液体体积占烧瓶球形容器的1/4-2/3,不可蒸干82、重结晶选择适当的溶剂,要求该溶剂:(1)杂质在溶剂中溶解度很小或很大,易于除去;(2)被提纯的有机物的溶解度,受温度的影响较大
该有机物在热溶液中溶解度较大,冷溶液中的溶解度较小,冷却后易于结晶析出实验1-2:苯甲酸的重结晶(C6H5-COOH25℃(0
17g)95℃(6