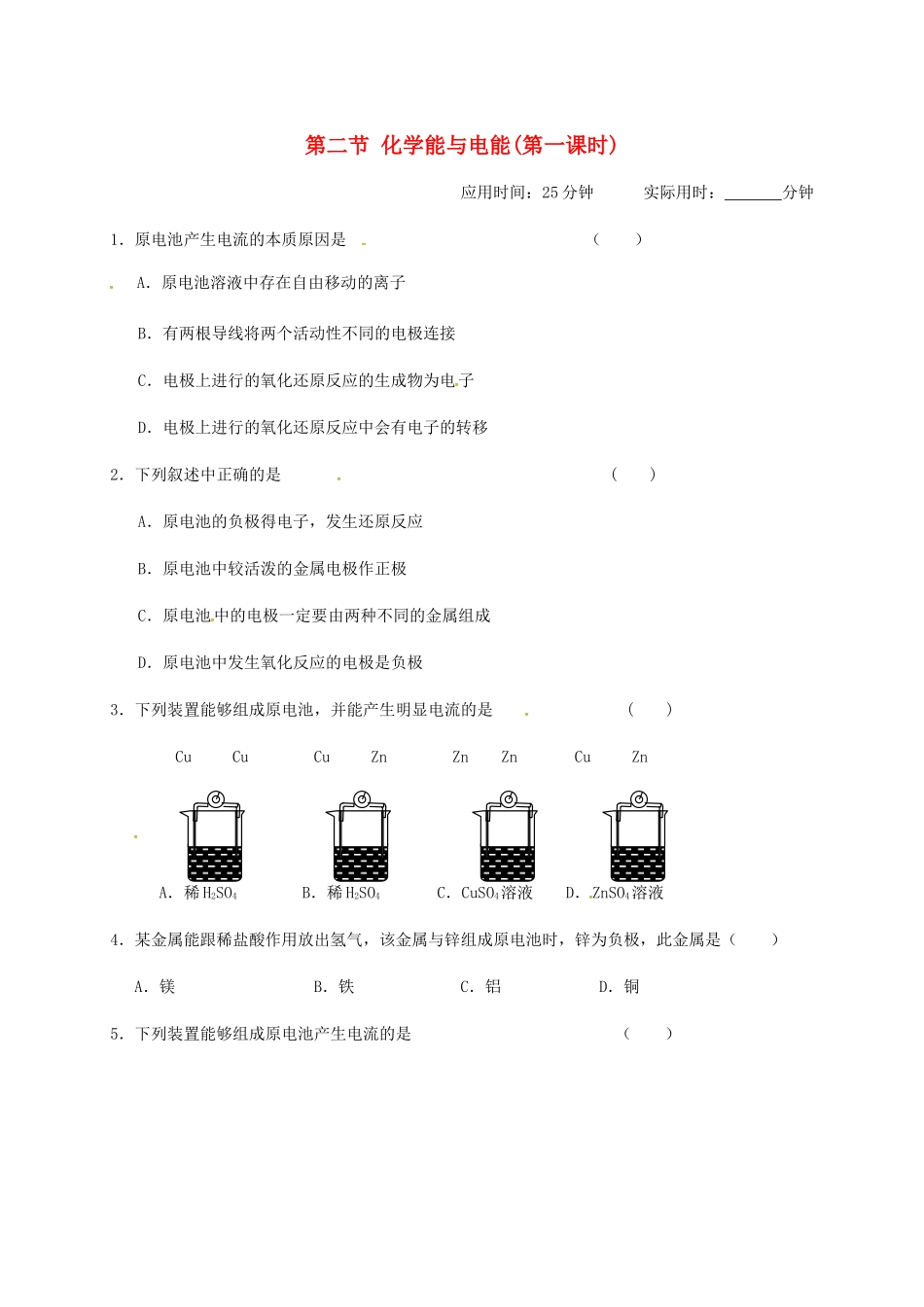
第二节化学能与电能(第一课时)应用时间:25分钟实际用时:分钟1.原电池产生电流的本质原因是()A.原电池溶液中存在自由移动的离子B.有两根导线将两个活动性不同的电极连接C.电极上进行的氧化还原反应的生成物为电子D.电极上进行的氧化还原反应中会有电子的转移2.下列叙述中正确的是()A.原电池的负极得电子,发生还原反应B.原电池中较活泼的金属电极作正极C.原电池中的电极一定要由两种不同的金属组成D.原电池中发生氧化反应的电极是负极3.下列装置能够组成原电池,并能产生明显电流的是()CuCuCuZnZnZnCuZnA.稀H2SO4B.稀H2SO4C.CuSO4溶液D.ZnSO4溶液4.某金属能跟稀盐酸作用放出氢气,该金属与锌组成原电池时,锌为负极,此金属是()A.镁B.铁C.铝D.铜5.下列装置能够组成原电池产生电流的是()6.在用Zn片、Cu片和稀硫酸组成的原电池装置中,工作一段时间后,下列说法正确的是()A.锌片是正极,铜片上有气泡产生B.电流方向是从锌片流向铜片C.溶液中硫酸的物质的量浓度减小D.电解质溶液的pH保持不变7.下列各装置中,烧杯中盛有海水,能够形成原电池并且铁为正极的是()、、ABCD8.在铜锌硫酸原电池中,锌为极,电子,电极发生的是反应(填氧化或还原),电极反应式为;铜为极,电子,电极发生的是反应,电极反应式为,铜片上观察到的现象为
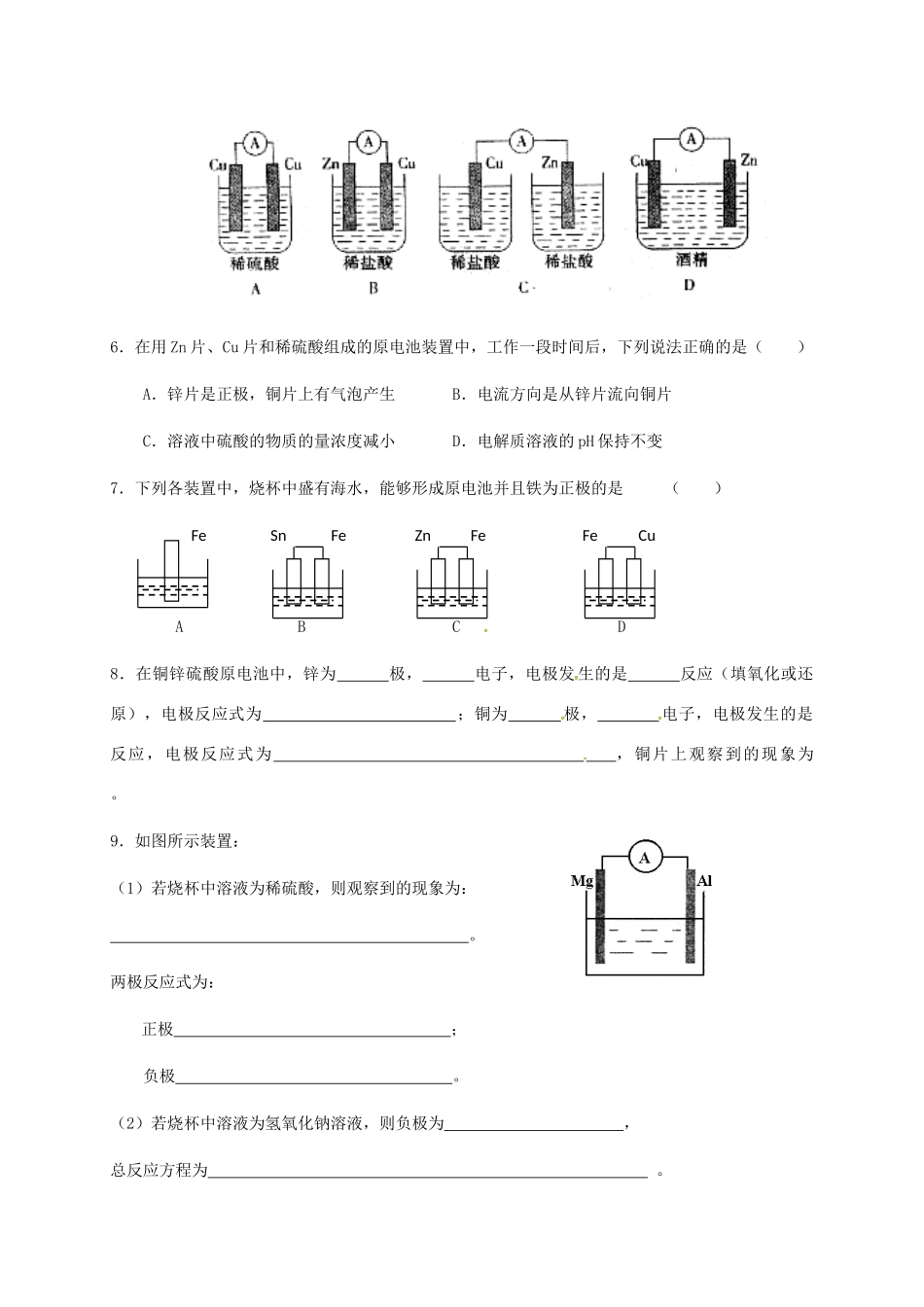
9.如图所示装置:(1)若烧杯中溶液为稀硫酸,则观察到的现象为:
两极反应式为:正极;负极
(2)若烧杯中溶液为氢氧化钠溶液,则负极为,总反应方程为
CuFeFeZnFeFeSn10.利用Cu+2FeCl3=CuCl2+2FeCl2反应,设计一个原电池,画出示意图,并写出正、负极的电极反应式