第二节化学计量在实验中的应用第1课时物质的量的单位——摩尔1.物质的量及其单位——摩尔(1)物质的量:国际单位制中的7个基本物理量之一,它表示含有一定数目粒子的集合体,符号为n
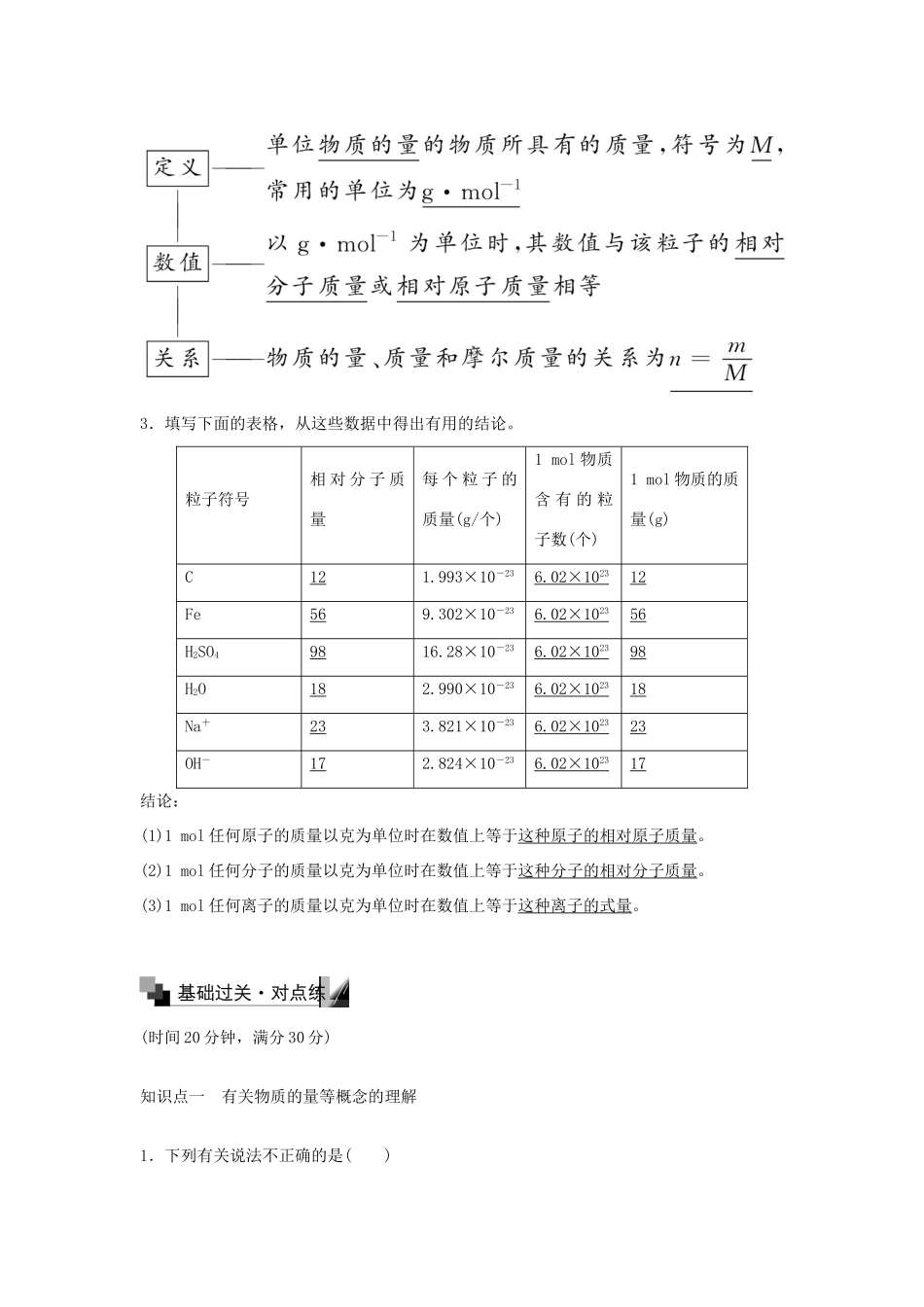
(2)物质的量的单位——摩尔(3)阿伏加德罗常数2.摩尔质量3.填写下面的表格,从这些数据中得出有用的结论
粒子符号相对分子质量每个粒子的质量(g/个)1mol物质含有的粒子数(个)1mol物质的质量(g)C121
993×10-236
02×102312Fe569
302×10-236
02×102356H2SO49816
28×10-236
02×102398H2O182
990×10-236
02×102318Na+233
821×10-236
02×102323OH-172
824×10-236
02×102317结论:(1)1mol任何原子的质量以克为单位时在数值上等于这种原子的相对原子质量
(2)1mol任何分子的质量以克为单位时在数值上等于这种分子的相对分子质量
(3)1mol任何离子的质量以克为单位时在数值上等于这种离子的式量
(时间20分钟,满分30分)知识点一有关物质的量等概念的理解1.下列有关说法不正确的是()A.物质的量表示含有一定数目粒子的集合体B.物质的量是联系微观粒子和宏观物质的物理量C.0
012kg12C中所含碳原子数约为6
02×1023D.物质的量可用于表示宏观物质的多少答案:D解析:B项,物质的量是联系微观粒子和宏观物质的桥梁
D项,物质的量不适用于宏观物质
2.下列叙述正确的是()A.1mol任何物质中都含有NA个分子B.摩尔是物质的量的单位C.摩尔是一个基本物理量D.摩尔是表示物质数量的单位答案:B解析:A项,要看构成该物质的粒子是分子、原子还是离子
B项,摩尔是物质的量的单位
C项,摩尔是国际单位制中的基本单位之一
3.下列有关物质的量和摩尔的叙述不正确