第2课时铝与氢氧化钠溶液的反应物质的量在化学方程式计算中的应用课程目标1.掌握铝与强酸、强碱反应的性质
2.掌握物质的量与其他物理量的换算关系
3.掌握物质的量在化学方程式计算中的应用
4.了解化学计算中的常用方法
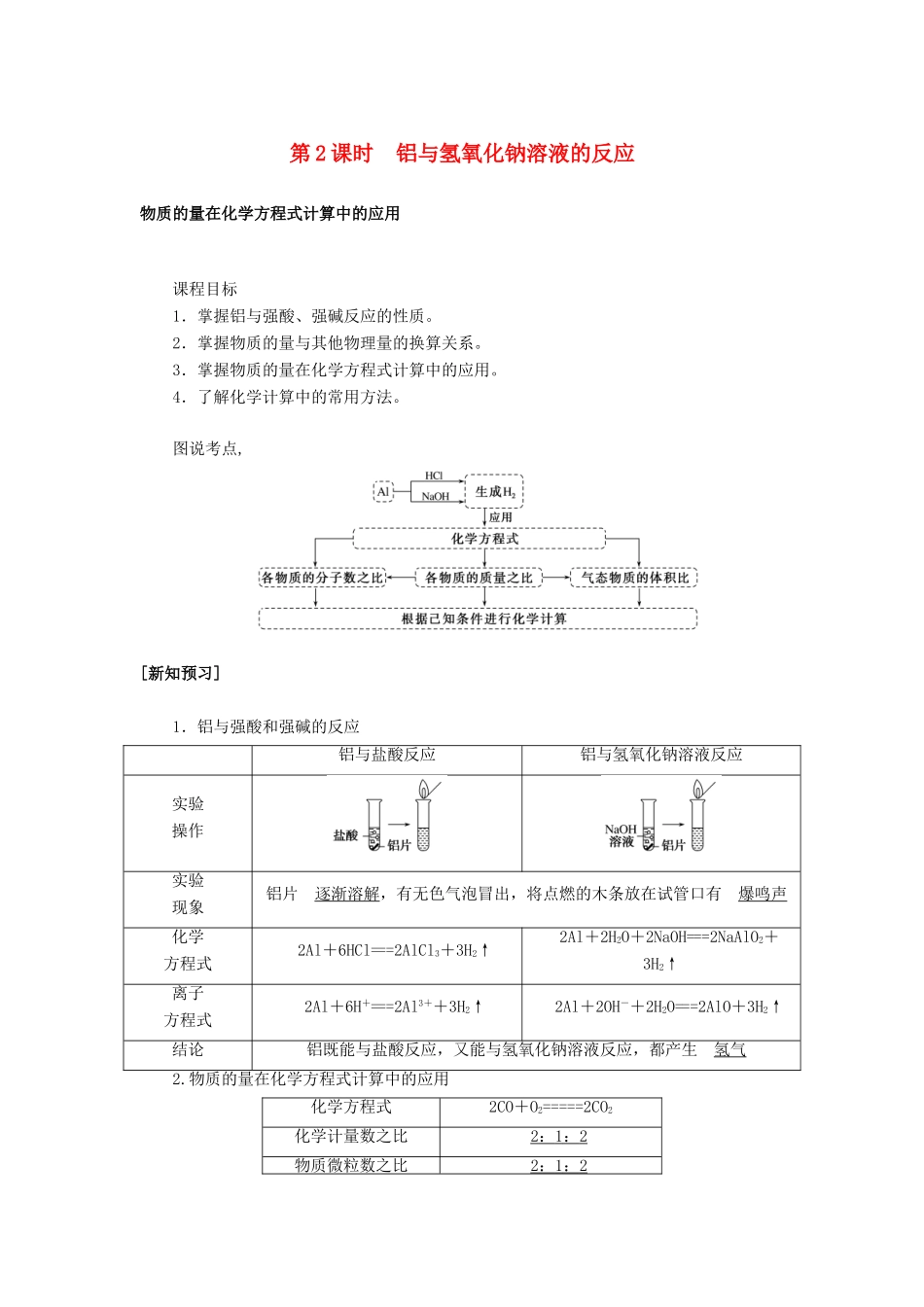
图说考点,[新知预习]1.铝与强酸和强碱的反应铝与盐酸反应铝与氢氧化钠溶液反应实验操作实验现象铝片逐渐溶解,有无色气泡冒出,将点燃的木条放在试管口有爆鸣声化学方程式2Al+6HCl===2AlCl3+3H2↑2Al+2H2O+2NaOH===2NaAlO2+3H2↑离子方程式2Al+6H+===2Al3++3H2↑2Al+2OH-+2H2O===2AlO+3H2↑结论铝既能与盐酸反应,又能与氢氧化钠溶液反应,都产生氢气2
物质的量在化学方程式计算中的应用化学方程式2CO+O2=====2CO2化学计量数之比2:1:2物质微粒数之比2:1:2扩大NA倍之后2NA:NA:2NA物质的量之比2_mol:1_mol:2_mol标准状况下体积之比44
8_L:22
4_L:44
8_L相同状况下体积之比2:1:2结论:化学方程式中化学计量数之比=各物质的物质的量之比=各物质微粒数目之比
[即时性自测]1.判断正误,正确的打“√”,错误的打“×”(1)等质量的Al与足量的盐酸、NaOH溶液充分反应,生成的H2的物质的量相同
()(2)同浓度同体积的盐酸、NaOH溶液与足量Al充分反应,生成的H2的物质的量相同
()(3)化学方程式4Na+O2===2Na2O可表示4mol钠原子和1mol氧气分子反应生成2mol氧化钠
()(4)根据离子方程式Mg+2H+===Mg2++H2↑可知1g镁与足量氢离子反应可生成1mol氢气
()(5)化学反应前后物质的质量和物质的量均不变
()答案:(1)√(2)×(3)√(4)×(5)×2.对于铝和烧碱溶液的反应,下列说法不