知识回顾:一、离子键11、、,称为离子键
2、成键的微粒:阴、阳离子3、成键的本质:阴阳离子间的阴阳离子间的静电静电作用作用使带相反电荷的阴阳离子结合的相互(静电)作用思考:这些微粒之间的静电作用包括哪些
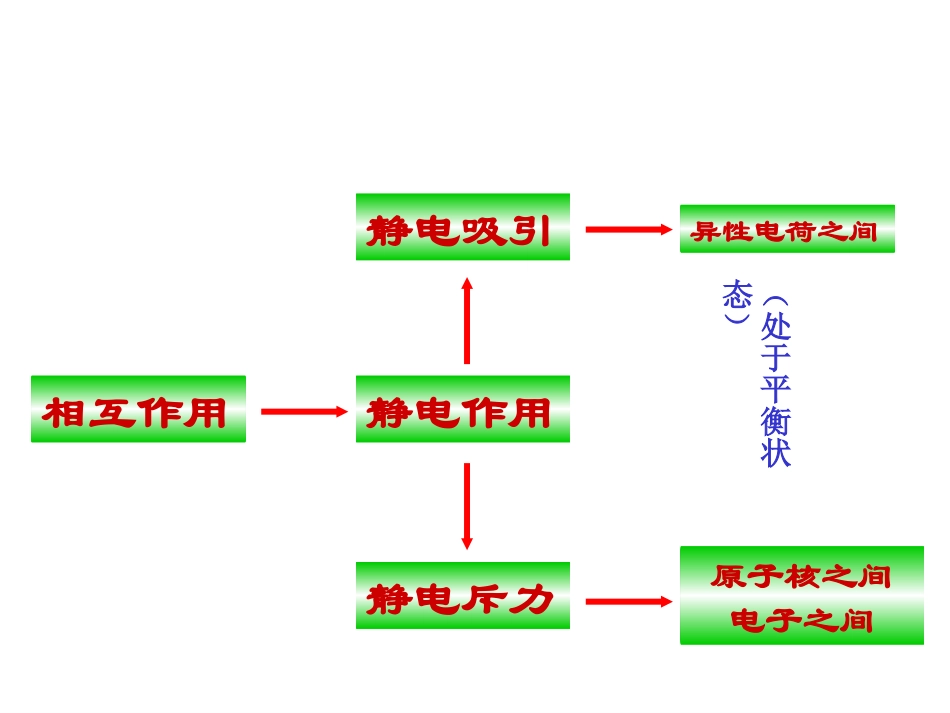
相互作用静电作用静电吸引静电斥力异性电荷之间原子核之间电子之间(处于平衡状态)—+Na和Cl的反应+_+++++______Na和Cl的反应根据下列数据判断:元素之间两两是否可以形成离子键
提示:一般认为,当电负性差值_____时原子间才有可能形成离子键
7元素KMgAlClSFO数据0
44交流讨论思考思考1、活泼的金属元素(IA、IIA)和活泼的非金属元素(VIA、VIIA)形成的化合物
2、活泼的金属元素和酸根离子(或氢氧根离子)形成的化合物3、铵根和酸根离子(或活泼非金属元素离子)形成的盐
4、成键的条件:离子的电子式阳离子的表示阴离子的表示Cl××××[]-××××××××[]2-××××O二、用电子式表示离子化合物的形成Na+Mg2+化合物的电子式如NaCl的电子式Na+Cl××××[]-××××如MgO电子式××××[]2-××××OMg2+小结:离子化合物电子式的书写ClNaNaO2-NaClMg2Cl1
简单阴离子的电子式不但要表达出最外层所有电子数(包括得到的电子),而且用方括号“[]”括起来,并在右上角注明负电荷数3
离子化合物的电子式由阴离子和阳离子电子式组成,相同的离子不能合并2
简单阳离子的电子式就是离子符号用电子式表示NaCl的形成过程
Na×+Cl×××××Na+Cl××××[]-××××××小结:用电子式表示离子键的形成过程SKK3
用表示电子转移的方向S2-K+K+1
左边是组成离子化合物的各原子的电子式,右边是离子化合物的电子式2
连接号为“”Na+Cl-Cl-Na+N