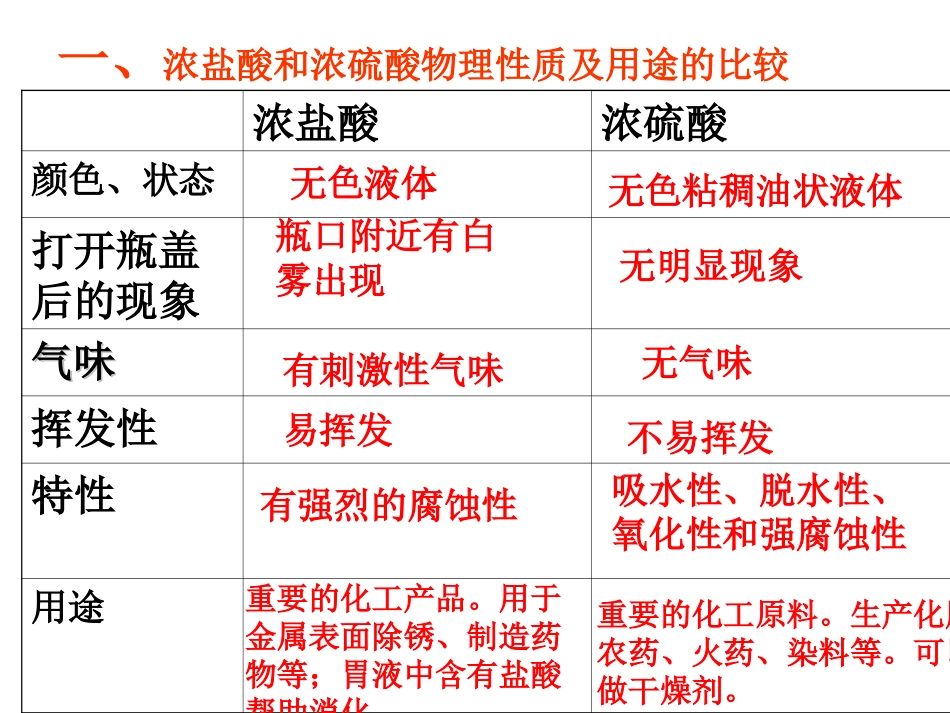
酸和碱复习课常见的酸和碱复习课一、浓盐酸和浓硫酸物理性质及用途的比较浓盐酸浓硫酸颜色、状态打开瓶盖后的现象气味气味挥发性特性用途无色液体无色粘稠油状液体瓶口附近有白雾出现无明显现象有刺激性气味无气味易挥发不易挥发有强烈的腐蚀性吸水性、脱水性、氧化性和强腐蚀性重要的化工产品
用于金属表面除锈、制造药物等;胃液中含有盐酸帮助消化重要的化工原料
生产化肥、农药、火药、染料等
可以做干燥剂
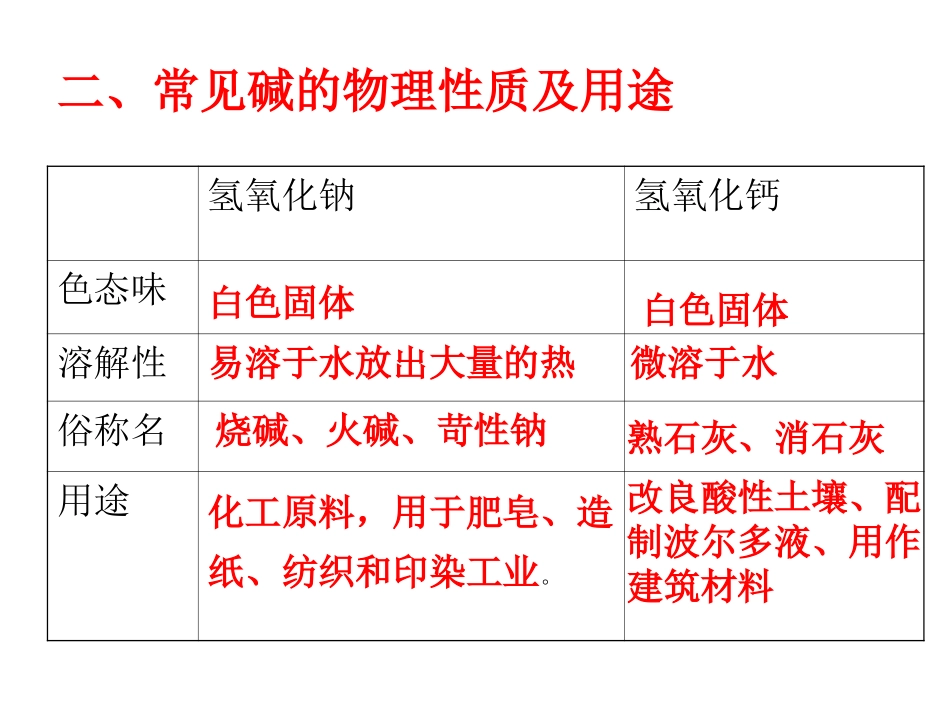
二、常见碱的物理性质及用途氢氧化钠氢氧化钙色态味溶解性俗称名用途白色固体白色固体易溶于水放出大量的热微溶于水烧碱、火碱、苛性钠熟石灰、消石灰化工原料,用于肥皂、造纸、纺织和印染工业
改良酸性土壤、配制波尔多液、用作建筑材料练一练•1、浓硫酸和浓盐酸敞口放置,溶质质量分数都会,但是原因不同,浓盐酸是因为,浓硫酸是因为
•在表面皿上放一些固体烧碱,露置在空气中,可以观察到的象,其原因是
增大具有挥发性,使溶质质量减小具有吸水性,使溶剂质量增加表面潮湿而逐渐溶解固体氢氧化钠具有吸水性三、稀盐酸(HCl)稀硫酸(H2SO4)化学性质•1、能与指示剂反应1、能与指示剂反应稀盐酸稀硫酸紫色石蕊溶液无色酚酞溶液红色红色无色无色2、能与多种活泼金属反应,生成盐和氢气与稀盐酸反应与稀硫酸反应镁锌铁Mg+2HCl=MgCl2+H2↑Mg+H2SO4=MgSO4+H2↑Zn+2HCl=ZnCl2+H2↑Zn+H2SO4=ZnSO4+H2↑Fe+2HCl=FeCl2+H2↑Fe+H2SO4=FeSO4+H2↑3:能与某些金属氧化物反应,生成盐和水
现象化学方程式铁锈+稀盐酸铁锈+稀硫酸氧化铜+稀盐酸氧化铜+稀硫酸溶液由无色逐渐成黄色,红色固体逐渐消失溶液由无色逐渐变成蓝色,黑色固体逐渐消失
Fe2O3+6HCl=2FeCl3+3H2OFe2O3+3H2SO4=Fe2(SO4)3+3H2OCuO+2HCl=CuCl2+H