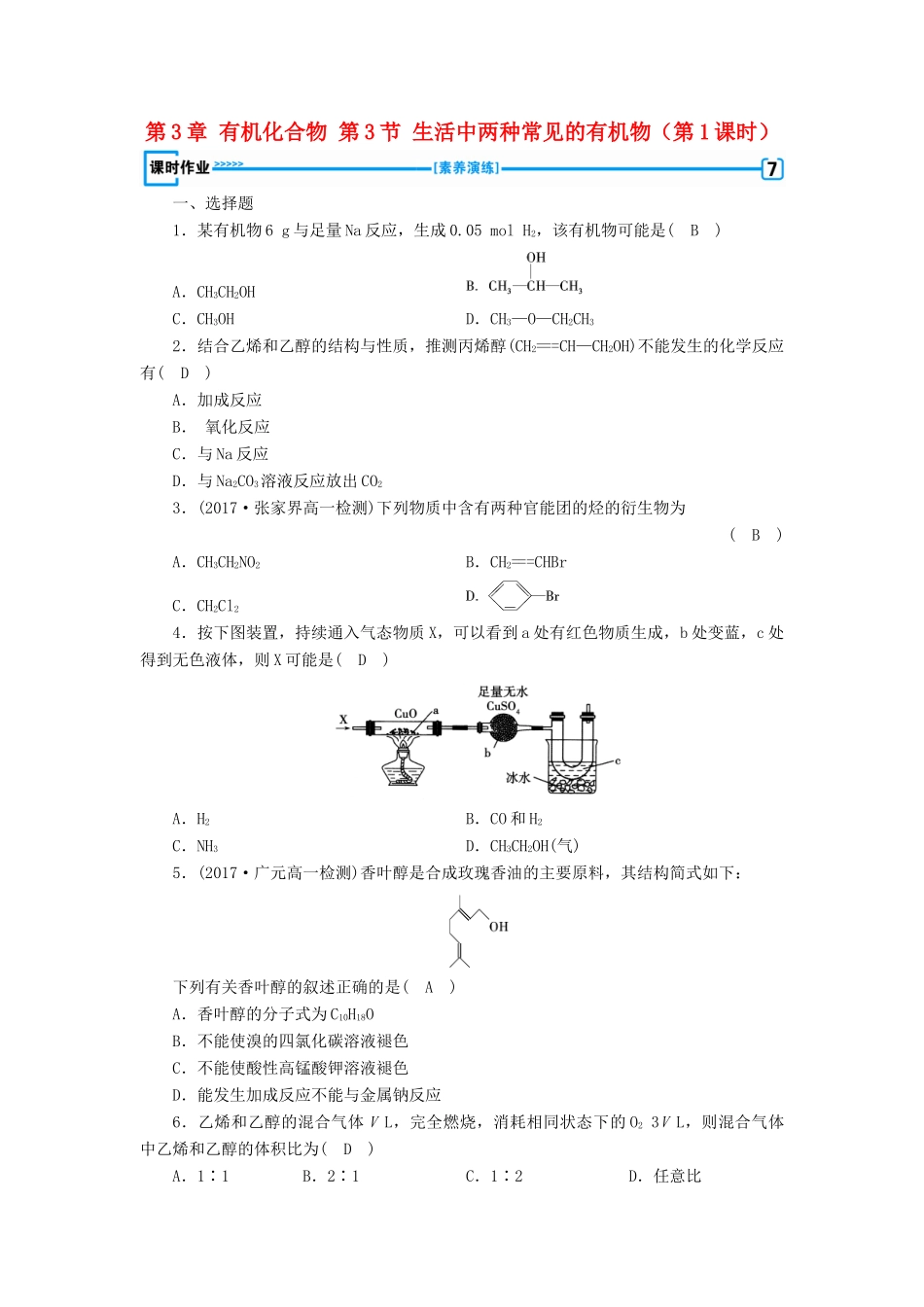
第3章有机化合物第3节生活中两种常见的有机物(第1课时)一、选择题1.某有机物6g与足量Na反应,生成0
05molH2,该有机物可能是(B)A.CH3CH2OHC.CH3OHD.CH3—O—CH2CH32.结合乙烯和乙醇的结构与性质,推测丙烯醇(CH2===CH—CH2OH)不能发生的化学反应有(D)A.加成反应B.氧化反应C.与Na反应D.与Na2CO3溶液反应放出CO23.(2017·张家界高一检测)下列物质中含有两种官能团的烃的衍生物为(B)A.CH3CH2NO2B.CH2===CHBrC.CH2Cl24.按下图装置,持续通入气态物质X,可以看到a处有红色物质生成,b处变蓝,c处得到无色液体,则X可能是(D)A.H2B.CO和H2C.NH3D.CH3CH2OH(气)5.(2017·广元高一检测)香叶醇是合成玫瑰香油的主要原料,其结构简式如下:下列有关香叶醇的叙述正确的是(A)A.香叶醇的分子式为C10H18OB.不能使溴的四氯化碳溶液褪色C.不能使酸性高锰酸钾溶液褪色D.能发生加成反应不能与金属钠反应6.乙烯和乙醇的混合气体VL,完全燃烧,消耗相同状态下的O23VL,则混合气体中乙烯和乙醇的体积比为(D)A.1∶1B.2∶1C.1∶2D.任意比7.(2017·雅安高一检测)区别乙醇、苯和溴苯,最简单的方法是(C)A.加酸性高锰酸钾溶液后振荡,静置B.与乙酸在有浓硫酸存在的条件下加热C.加蒸馏水后振荡,静置D.加硝酸银溶液后振荡,静置解析:物质检验最简单的方法是从物质物理性质如颜色、密度、溶解性等方面考虑
乙醇、苯、溴苯都是无色液体,外观不能鉴别,因此可以从溶解性、密度方面鉴别,所加最简单试剂即为蒸馏水,乙醇与水互溶,苯与水分层且油状物在上层,溴苯与水也分层但油状物在下层
8.下列选项中能说明乙醇(酒精)作为燃料的优点是(D)①燃烧时发生氧化反应②充分燃烧的产物不污染