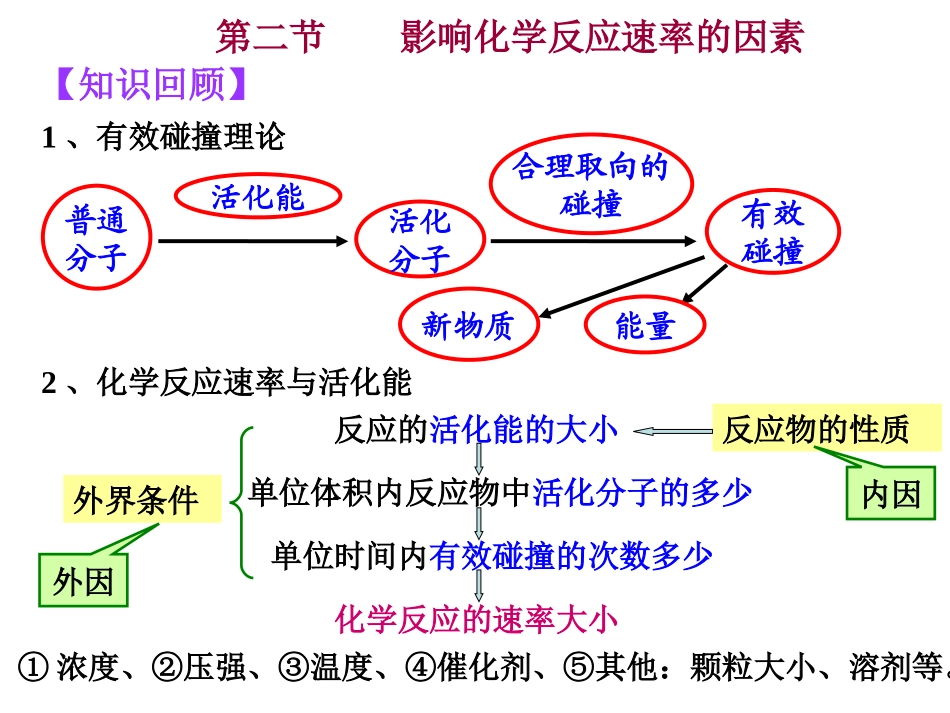
第二节影响化学反应速率的因素【知识回顾】1、有效碰撞理论普通分子活化能活化分子合理取向的碰撞有效碰撞新物质能量2、化学反应速率与活化能化学反应的速率大小单位时间内有效碰撞的次数多少单位体积内反应物中活化分子的多少反应的活化能的大小反应物的性质内因外界条件外因①浓度、②压强、③温度、④催化剂、⑤其他:颗粒大小、溶剂等
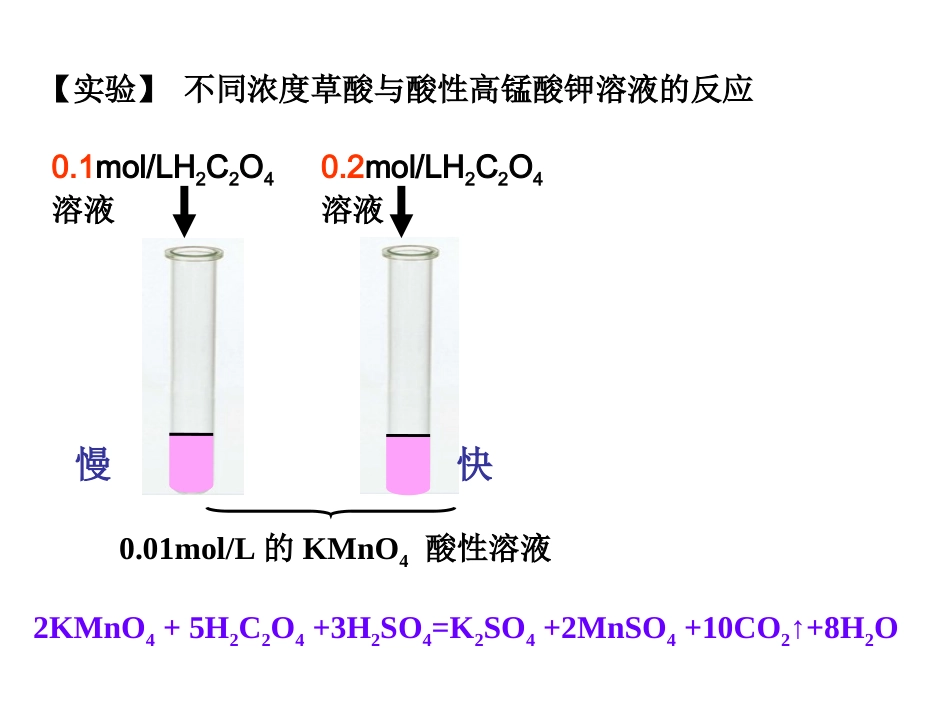
01mol/L的KMnO4酸性溶液0
1mol/LH2C2O4溶液0
2mol/LH2C2O4溶液快慢【实验】不同浓度草酸与酸性高锰酸钾溶液的反应2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O一、浓度对反应速率的影响当其他条件不变时,增大反应物的浓度,化学反应速率增大
减小反应物的浓度,化学反应速率减小
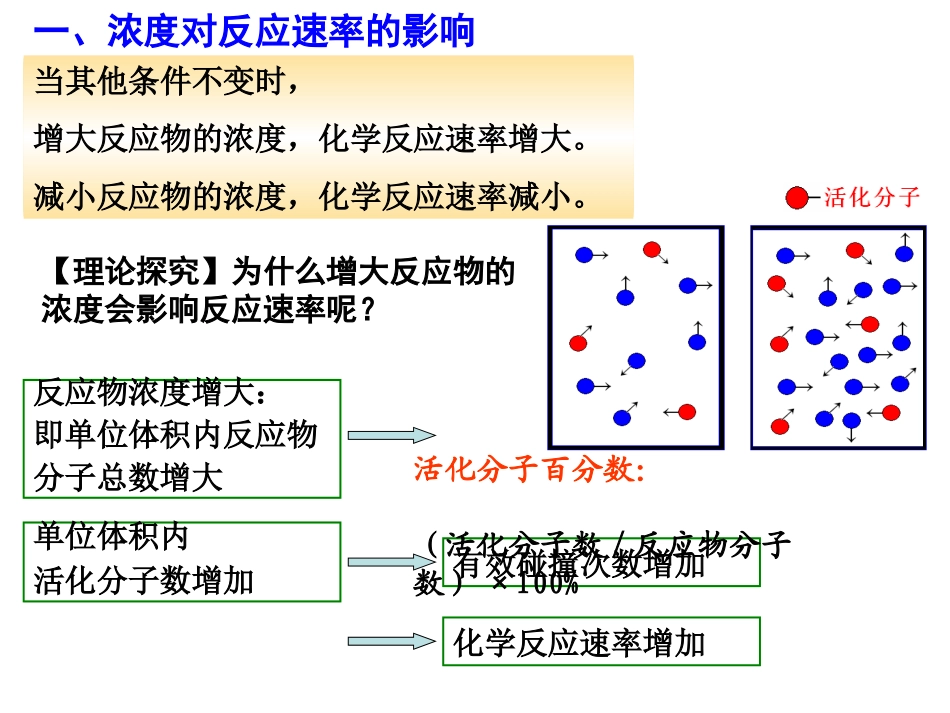
【理论探究】为什么增大反应物的浓度会影响反应速率呢
反应物浓度增大:即单位体积内反应物分子总数增大单位体积内活化分子数增加有效碰撞次数增加化学反应速率增加活化分子百分数:(活化分子数/反应物分子数)×100%【注意】a
反应物是纯液体或固体,其浓度是常数,因此改变它们的量反应速率不变
一般来说,固体反应物表面积越大,反应速率越大
讨论1:把下列四种X溶液,分别加进四个盛有10mL、2mol/L的盐酸的烧杯中,并且均加水稀释至50mL,此时,X和盐酸缓缓地进行反应,其中反应速率最快的是()A10mL2mol/LB20mL2mol/LC10mL4mol/LD20mL3mol/L讨论2:恒温恒容的容器中进行反应N2O4(g)若反应物浓度由0
1mol/L降到0
06mol/L需20s,那么,反应物浓度由0
06mol/L降到0
024mol/L,需反应的时间为()A.等于18sB.等于12sC.大于18sD.小于18s2NO2(g)H△>0,二、压强对反应速率的影响对有气体参加或生成的反应增大压强相当于增大气体的浓