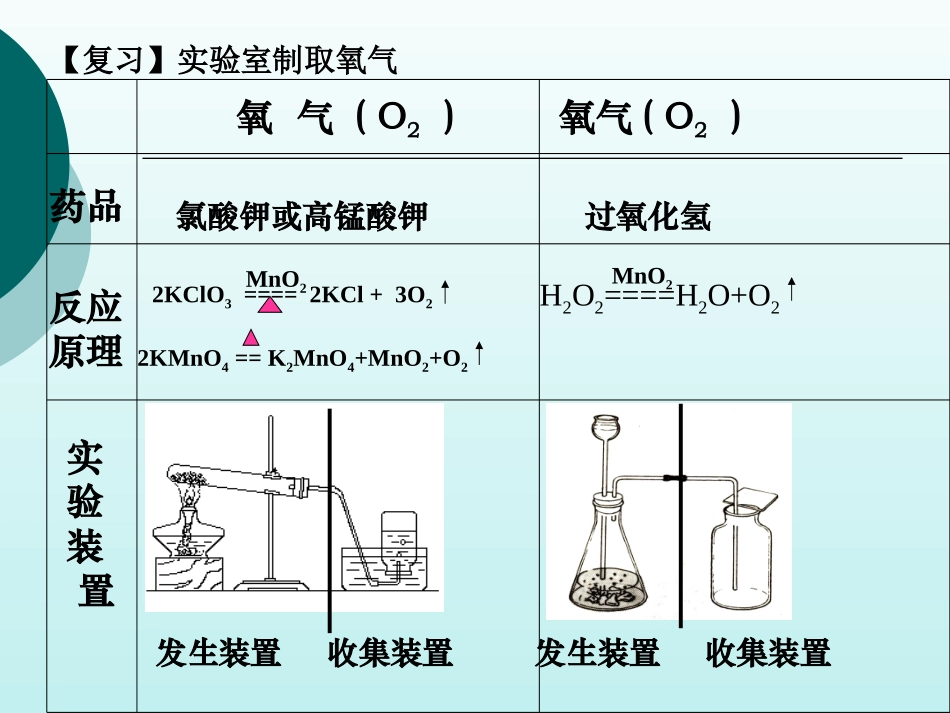
第六单元第二节长郡梅溪湖中学化学组一、写出下列物质的化学式:碳酸钙碳酸钠硫酸盐酸二、写出下列反应的化学方程式:1.实验室用过氧化氢和二氧化锰制取氧气。2.实验室用高锰酸钾加热制氧气。3.碳还原氧化铜课前练习:2KClO3====2KCl+3O2MnO22KMnO4==K2MnO4+MnO2+O2氯酸钾或高锰酸钾过氧化氢发生装置收集装置反应原理实验装置药品氧气(O2)氧气(O2)【复习】实验室制取氧气H2O2====H2O+O2MnO2发生装置收集装置氧气收集方法验证气体是氧气:检验氧气已集满排水法(氧气不易溶于水)向上排气法(氧气的密度比空气略大)带火星的木条伸入集气瓶,木条复燃带火星的木条放在集气瓶,瓶口,木条复燃一、药品:石灰石或大理石(主要成份为CaCO3)二、反应原理:CaCO3+2HCl==H2CO3+CaCl2H2CO3==H2O+CO2总反应:CaCO3+2HCl==CaCl2+H2O+CO2课题2二氧化碳制取的研究和稀盐酸可以用硫酸钙代替碳酸钙吗?可以用碳酸钠、碳酸氢钠代替碳酸钙吗?能用碳酸钙粉末代替块状的大理石(主要成分是碳酸钙)?能用浓盐酸代替稀盐酸吗?反应的生成物硫酸钙微溶于水,会包裹在大理石表面,阻碍反应的进一步进行。反应速率太快,收集时不便于操作。浓盐酸挥发性强,会使收集到的二氧化碳气体不纯。确定药品的原则:反应速率适中制取的气体纯净原料要廉价易得制取气体的装置:从两个方面考虑:(1)反应的条件。(2)药品的状态。2、在选择发生装置时要考虑哪些因素?2、在选择收集装置时应以什么为依据?主要应以物理性质两个方面:(1)气体在水中的溶解性(2)气体的密度与空气比较排水法向上排气法向下排气法CO2收集方法:向上排气法(CO2的密度比空气大)不能用排水法(CO2能溶于水,且与水发生反应)收集仪器:1、集气瓶2、玻璃片实验室制取二氧化碳主要仪器和药品请你根据书本提供的仪器,设计制取二氧化碳需要的装置实验室制取和收集二氧化碳的装置3、放置:4、检验方法:将气体通入澄清的石灰水,石灰水变浑浊,证明该气体是二氧化碳。盖上玻璃片正放5、验满方法:将燃着的木条放在集气瓶口,火焰熄灭,证明二氧化碳已收集满。课题总结1、实验室制取二氧化碳的反应原理CaCO3+2HCl=CaCl2+H2O+CO2↑2、药品:石灰石(或大理石)与稀盐酸3、反应装置:固体与液体在常温下反应的装置(与用过氧化氢制取氧气的装置相似)4、收集方法:只能用向上排空气法收集(为什么)5、检验二氧化碳的方法:气体通入澄清的石灰水,石灰水变浑浊,说明是二氧化碳。6、验满方法:燃烧的木条平放在集气瓶口,木条熄灭,说明已收集满。1.装置的选择2、下列制取二氧化碳的装置有哪些错误?A.长颈漏斗下端管口没有插到液面以下。B.广口瓶内导气管插到液面以下。C.用向下排气法收集。D.集气瓶内导管没有插到集气瓶底部。E.集气瓶口没有放玻片思考:1、如果用浓盐酸代替稀盐酸与石灰石反应制取CO2行不行?答:不行,因为浓盐酸易挥发,使制得的二氧化碳气体中含有较多的氯化氢气体,导致CO2不纯。2、实验室为何不用碳酸钙粉末跟稀盐酸反应制取CO2?答:碳酸钙粉末跟稀盐酸反应生成CO2,但反应速度太快,不利于收集,因此不用于实验室制取CO2气体。不能用。因为开始时生成微溶于水的硫酸钙薄膜,附着在石灰石的表面,使它不能接触到稀硫酸,阻止反应继续进行。3、可否用硫酸代替盐酸与石灰石反应制CO2,为什么?有以下几种反应可产生二氧化碳,你认为哪种更适合实验室制取二氧化碳?为什么?1、用碳酸钙和稀盐酸2、用碳酸钙和稀硫酸3、用碳酸钠和稀硫酸4、木炭的燃烧课外作业:作业《聚焦课堂》P68-69