7自然资源的开发利用期末复习【考向分析】本章知识紧紧围绕金属矿物、海水和化石燃料这些重要自然资源综合利用中的化学基本原理和基础知识,关注自然资源开发和社会可持续发展这一当今社会热点问题,努力揭示化学在面对和解决这一问题中的作用和价值,如环境监测、绿色化学等
题型多为选择题、实验综合题和化学工艺流程题,试题主要考查无机物之间的转化,如在固态下和液态下,金属及其化合物、非金属及其化合物之间的反应,涉及氧化还原反应和离子反应的应用;有机物之间的转化,如加聚、裂化等;常用的分离物质的方法,如蒸馏法、结晶法、过滤法、分液法、萃取法等;常用的实验操作,如浸取、洗涤、蒸发浓缩等
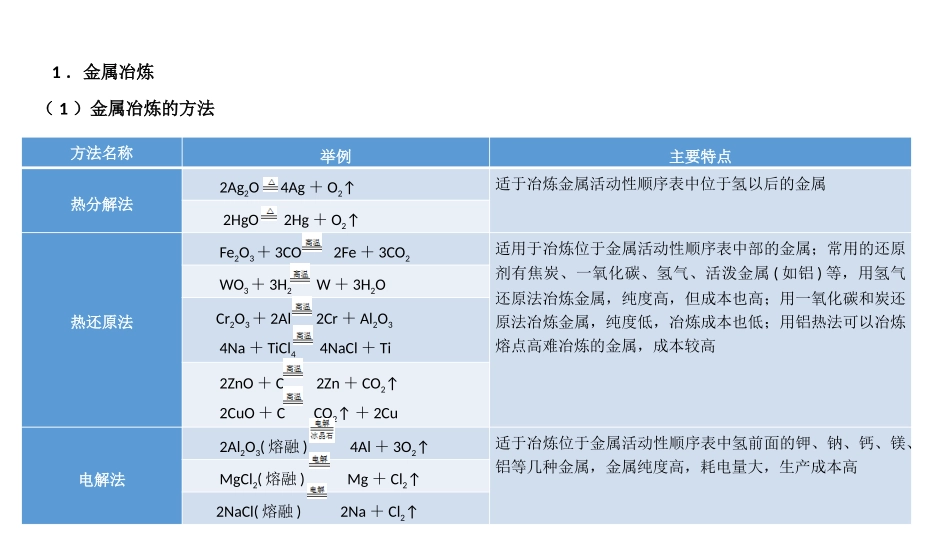
1.金属冶炼(1)金属冶炼的方法方法名称举例主要特点热分解法2Ag2O4Ag+O2↑适于冶炼金属活动性顺序表中位于氢以后的金属2HgO2Hg+O2↑热还原法Fe2O3+3CO2Fe+3CO2适用于冶炼位于金属活动性顺序表中部的金属;常用的还原剂有焦炭、一氧化碳、氢气、活泼金属(如铝)等,用氢气还原法冶炼金属,纯度高,但成本也高;用一氧化碳和炭还原法冶炼金属,纯度低,冶炼成本也低;用铝热法可以冶炼熔点高难冶炼的金属,成本较高WO3+3H2W+3H2OCr2O3+2Al2Cr+Al2O34Na+TiCl44NaCl+Ti2ZnO+C2Zn+CO2↑2CuO+CCO2↑+2Cu电解法2Al2O3(熔融)4Al+3O2↑适于冶炼位于金属活动性顺序表中氢前面的钾、钠、钙、镁、铝等几种金属,金属纯度高,耗电量大,生产成本高MgCl2(熔融)Mg+Cl2↑2NaCl(熔融)2Na+Cl2↑(2)铝热反应铝热反应铝和金属氧化物在高温下发生剧烈反应并放出大量热的化学反应反应原理Al作还原剂,难熔金属氧化物作氧化剂,用铝将金属氧化物中的金属置换出来铝热剂铝粉和某些难熔金属氧化物(Fe3O4、Cr2O3、V2O5等)组成的混合物实