新课标人教版化学必修Ⅱ第二章第一节化学能与热能2、化学反应的本质是什么
化学反应的本质是旧化学键的断裂和新化学键的形成
1、什么是化学键
使离子相结合或原子相结合的强烈的作用力
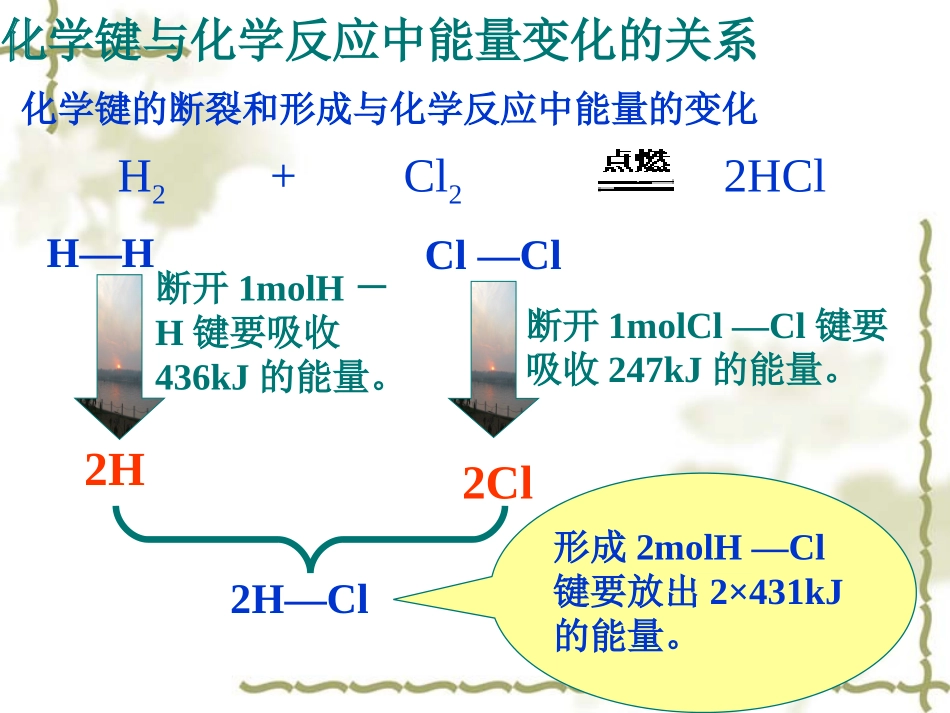
第一节化学能与热能化学键与化学反应中能量变化的关系化学键的断裂和形成与化学反应中能量的变化2HH—HCl—ClH2+Cl22HCl断开1molH-H键要吸收436kJ的能量
断开1molCl—Cl键要吸收247kJ的能量
2Cl2H—Cl形成2molH—Cl键要放出2×431kJ的能量
在反应H2+Cl2=2HCl中,已知1molH-H断开要吸收436kJ的能量,1molCl-Cl断开要吸收247kJ的能量,1molH-Cl形成时放出431kJ的能量,判断该反应是反应放热(1)化学键断裂时需要吸收能量
吸收总能量为:436kJ+247kJ=683kJ,(2)化学键形成时需要释放能量
释放总能量为:431kJ+431kJ=862kJ,(3)反应中放出的能量的计算:862kJ—683kJ=179kJ化学键的断裂和形成是化学反应中能量变化的主要原因
1、化学反应中能量变化的主要原因是什么
2、化学反应中能量变化与化学键的关系是什么呢
化学反应中是吸收能量还是放出能量要看断键时吸收的能量多还是成键时放出能量得多
化学反应中能量变化的原因(1)从化学反应的本质角度考虑(微观)断键吸收的总能量成键放出的总能量化学反应放出能量化学反应吸收能量2molH2和1molO2生成2molH2O的能量变化(H与H键能是436KJ/mol,O与O键能是496KJ/mol,H与O键能是463KJ/mol)算一算:在101
3kPa,298K条件下,断开1molAB为A、B时过程的焓变(即能量的变化),称为A-B键的键能
通常,键能愈大,键愈牢固,由该键构成的分子也愈稳定,该分子本身所具有的能量就愈低
放出484KJ的能