第四章非金属及其化合物第四节氨硝酸硫酸第1课时氨1
掌握氨和铵盐的性质、用途
2.掌握氨气的实验室制法和铵根离子的检验
3.了解氮的循环及其对生态平衡的作用
4.理解由非金属单质、氢化物、氧化物、含氧酸等构成的非金属元素的知识体系
课前自主预习(学生用书P90)一、氨1.氮的固定多数生物不能直接从空气中吸收氮气,只能将氮转化为,才能被生物吸收
将的氮转为叫做氮的固定
目前工业上用和直接合成氨
反应方程式为
2.氨的物理性质氨是色、有气味、极易的气体
在常温下,1体积水大约可溶解体积的氨气
氨易,常用作
3.氨的化学性质(1)与H2O反应NH3溶于水中发生反应:NH3+H2O,其水溶液叫做
NH3·H2O不稳定,容易发生分解反应:NH3·H2O=====
氨水显碱性:NH3·H2O,能使酚酞溶液变红
简单表示为NH3+H2O+
(2)与酸反应生成铵盐:NH3+HCl===(产生白烟)
(3)NH3的催化氧化:4NH3+5O2=====+6H2O
、铵盐1.物理性质:铵盐都于水
2.化学性质(1)铵盐受热易分解NH4Cl受热分解的化学方程式:,NH4HCO3受热分解的化学方程式:
(2)铵盐与碱反应NaOH与NH4NO3反应的化学方程式:
三、氨的实验室制法1.在实验室中,常用加热的方法制取氨
2.常用来收集氨气
3.检验氨气用
学习与思考氨水和液氨中含有哪些粒子
提示液氨是氨气加压或降温得到的液态氨,是纯净物,只含有氨分子
氨水中存在NH3+H2ONH3·H2ONH+OH-,氨水中含有NH3、NH3·H2O、H2O、NH、OH-,还有水电离出的少量H+,所以氨水是混合物
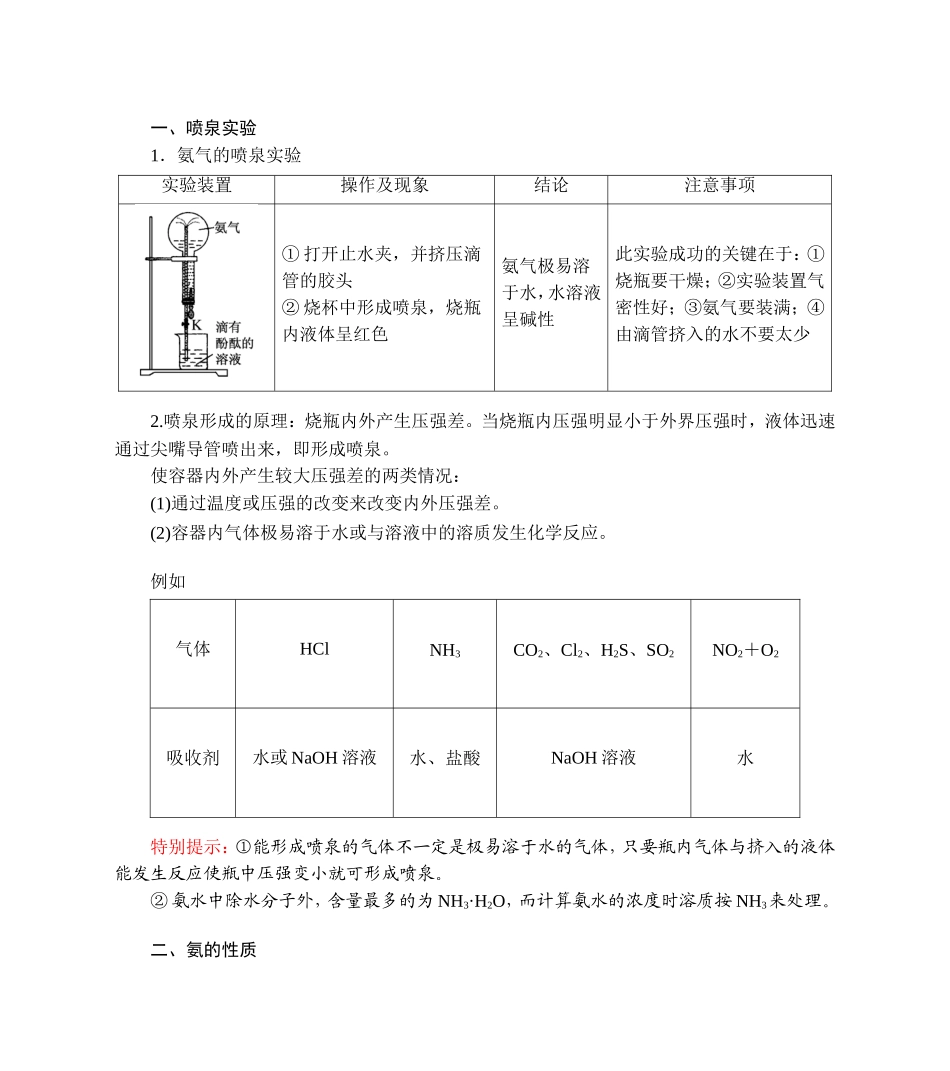
课堂深化探究(学生用书P90)一、喷泉实验1.氨气的喷泉实验实验装置操作及现象结论注意事项①打开止水夹,并挤压滴管的胶头②烧杯中形成喷泉,烧瓶内液体呈红色氨气极易溶于水,水溶液呈碱性此