电解原理及其应用(第一课时)1
什么是原电池
什么叫电解质
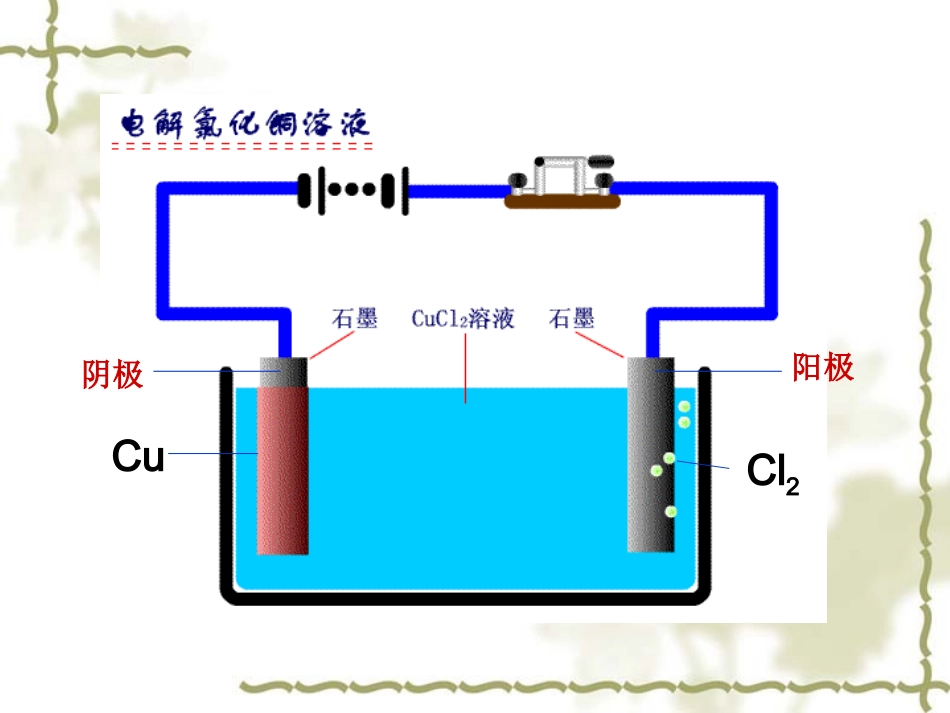
一、电解原理实验:电解CuCl2溶液:两根碳棒分别接电源正极和负极,一起插入CuCl2溶液中现象:阳极:有气泡产生
用湿润的碘化钾淀粉试纸检验(变蓝色)Cl2↑阴极:覆盖一层紫红色固体
Cu说明:在直流电流的作用下,电解质溶液发生了变化
阴极阳极CuCl2电解氯化铜溶液微观模拟电解原理1
电解:使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程叫做电解
电解池:将电能转化为化学能的装置
电解池的结构:阴极----与外电源的负极相连;阳极----与外电源的正极相连
分析电解反应(用惰性电极时)的一般思路:明确溶液中存在哪些离子根据阳极氧化、阴极还原以及氧化性、还原性强弱判断反应的离子先后,最后分析得出产物阴阳两极附近有哪些离子阳极:(Cl-、OH-)阴极:(Cu2+、H+)CuCl2Cu+Cl2↑电解2Cl--2e-=Cl2↑Cu2++2e-=Cu总反应式:(氧化反应)(还原反应)电解质的浓度,溶液的PH
若要使电解质溶液复原,怎么办
加CuCl25
电解CuCl2溶液:变小减小6
常见阴阳离子放电顺序:阳离子放电(得电子)由难到易(在阴极,发生还原反应)KK++CaCa2+2+NaNa++MgMg2+2+AlAl3+3+(H(H++))水中ZnZn2+2+FeFe2+2+PbPb2+2+(H(H++))酸中CuCu2+2+FeFe3+3+HgHg2+2+AgAg++•阴离子放电放电(失电子)由难到易由难到易::((在阳极在阳极,,发生氧化反应发生氧化反应))FF--ROROmmnn--OHOH--ClCl--BrBr--II--SS22--原电池电解池定义(能量)化学能转变成电能的装置
将电能转变成化学能的装置
形成条件①活动性不同两电极(燃料电池电极除外)②电解质溶液(有选择性)③两电极必