第二课时 弱电解质的电离思考冰醋酸加水稀释,醋酸在稀释的过程中微粒的变化包含哪些过程
CHCH33COOH COOH CHCH33COO COO - - + + HH++电离结合 C(H+)C(Ac-) C(HAc)HAc 初溶于水紧接着最后醋酸在电离过程中各微粒浓度的变化1 、弱电解质的电离 CHCH33COOH COOH CHCH33COO COO - - + H+ H++离子化分子化00最大不变不变不变 开始时开始时 VV 离子化 离子化 和 和 VV 分子化分子化怎样变化
当当 VV 离子化 离子化 = V= V 分子化分子化时,可逆过程达时,可逆过程达到一种什么样的状态
到一种什么样的状态
你能画出这个过程的你能画出这个过程的 VV ~~ tt 图吗
反应速率V( 电离 )V( 结合 )V( 电离 ) = V( 结合 ) 电离平衡状态弱电解质电离平衡状态建立示意图时间22 、电离平衡状态建立、电离平衡状态建立电离平衡是一种 电离平衡是一种 化学平衡化学平衡 电离平衡状态是指 在一定条件下(如温度、浓度等)的弱电解质的溶液中,弱电解质分子电离成离子的速率和离子重新结合成分子的速率相等,溶液中各分子、离子的浓度保持不变的状态
前提实质标志 3
定义:定义: 44 、特点:、特点:电离平衡是一种动态平衡 条件不变,溶液中各分子、离子的浓度不变,溶液里既有离子又有分子 条件改变时,电离平衡发生移动
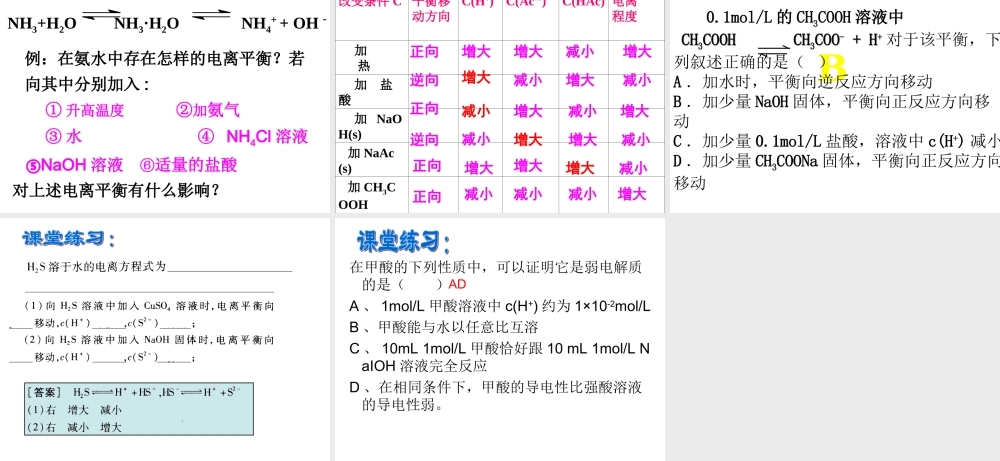
弱电解质的电离 V 电离 =V 结合≠ 0① 逆:② 等:③ 动: ④定:⑤ 变: 思考与交流(教材 p41 )根据化学平衡理论,分析一元弱酸(设为 HA )、一元弱碱(设为 BOH )的电离平衡过程,并完成下列问题:1 )、写出弱酸、弱碱的电离方程式: HA H+ + A- BOH B+ + OH- 2 )、结合图 3-3 填写下表00最大最大0