溶液的配制及分析0
1000mol··L-1NaOH 溶液25
00mL 未知浓度盐酸酸碱指示剂如何配制呢
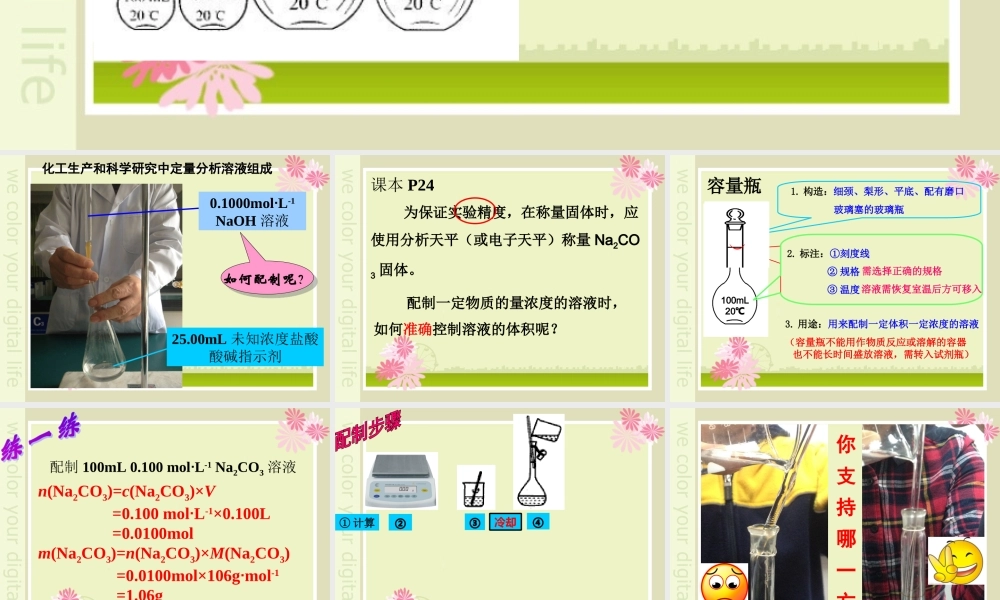
化工生产和科学研究中定量分析溶液组成课本 P24 为保证实验精度,在称量固体时,应使用分析天平(或电子天平)称量 Na2CO3 固体
配制一定物质的量浓度的溶液时,如何准确控制溶液的体积呢
构造:细颈、梨形、平底、配有磨口 玻璃塞的玻璃瓶2
标注:①刻度线 ② 规格 ③ 温度 需选择正确的规格3
用途:用来配制一定体积一定浓度的溶液(容量瓶不能用作物质反应或溶解的容器 也不能长时间盛放溶液,需转入试剂瓶)溶液需恢复室温后方可移入容量瓶100mL20℃) 配制 100mL 0
100 mol·L-1 Na2CO3 溶液n(Na2CO3)=c(Na2CO3)×V =0
100 mol·L-1×0
100L =0
0100molm(Na2CO3)=n(Na2CO3)×M(Na2CO3) =0
0100mol×106g·mol-1 =1
06g③④① 计算②冷却你 支 持 哪 一 方
两靠一不靠100mL20℃③④洗涤振荡⑤摇匀检查容量瓶是否漏水 怎么检查呢
① 计算②转移冷却配制一定物质的量浓度溶液的要求:质量精确{称量准确转移完全转移时用玻璃棒正确引流洗涤烧杯内壁和玻璃棒 2 ~3 次,并将洗涤液转入容量瓶
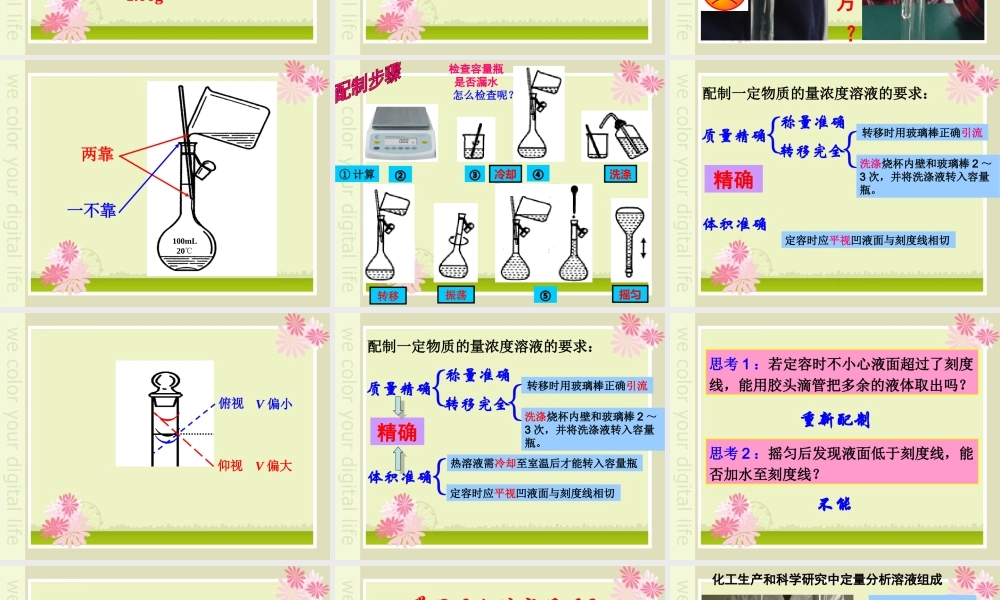
定容时应平视凹液面与刻度线相切{精确体积准确)))俯视仰视V 偏小V 偏大配制一定物质的量浓度溶液的要求:质量精确体积准确{称量准确转移完全转移时用玻璃棒正确引流洗涤烧杯内壁和玻璃棒 2 ~3 次,并将洗涤液转入容量瓶
热溶液需冷却至室温后才能转入容量瓶定容时应平视凹液面与刻度线相切{{精确思考 1 :若定容时不小心液面超过了刻度线,能用胶头滴管把多余的液体取出吗
思考 2 :摇匀后发现液面低于刻度线,能否加水至刻度线
重新配制不能 思考 3