教 学 设 计1 课题生活中两种常见的有机物(第一课时)学科化学授课教师李丽华单位宾县第二中学教学目标1、知识与技能:(1)了解乙醇的物理性质和在生产生活中的应用(2)掌握乙醇的分子结构和化学性质——与钠的反应、氧化反应
2、过程与方法:(1)通过实验探究,获得乙醇的结构、性质之间的关系
(2)通过有关乙醇的实验,提高观察化学实验现象、分析实验结果的能力
3、情感态度价值观:(1)通过比较乙烷和乙醇结构、性质的差异,认识官能团决定有机物的性质
(2)通过新旧知识的联系,培养知识迁移,进一步激发学习的兴趣
教学重点乙醇的结构和化学性质
教学难点乙醇的化学性质
教学方法实验---探究---讲解---练习
教师活动学生活动教学意图出示白酒、啤酒、红酒、酒精样品导入新课出示一瓶酒精让学生观察叙述物理性质教师适当补充
(一)乙醇的物理性质乙醇俗称酒精,通常情况下是无色、有特殊香味的液体,密度比水小,沸点 78
5℃,易挥发,能和水以任意比互溶,能溶解多种无机物和有机物
(二)乙醇分子组成和结构探究乙醇分子的结构:将 4
6g 有机物 A 完全燃烧后的产物依次通过盛足量浓硫酸的洗气瓶和足量碱石灰的干燥管,充分吸收后称量发现洗气瓶质量增重 5
4g,干燥管质量增重8
A 的密度是相同条件下 H2密度的 23 倍,试确定 A 的分子式
让学生写出乙醇的分子式
C2H6O让学生根据乙醇的分子组成推测乙醇的结构,写出乙醇分子可能的结构简式让学生动手插球棍模型定量实验探究乙醇的结构式实验用品:本实验的主要用品如图所示
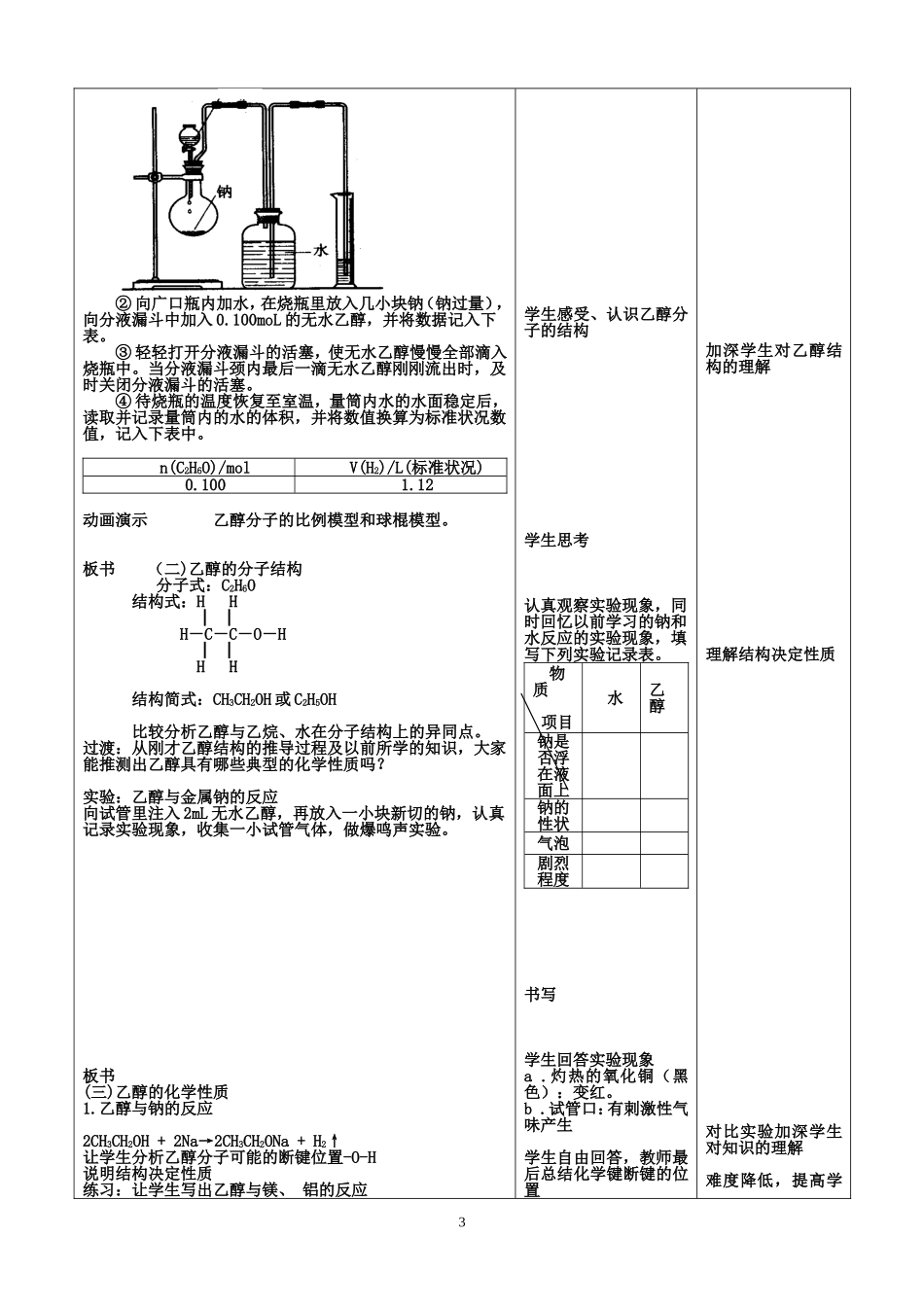
实验步骤:① 如下图所示组装各仪器,检验装置的气密性
观察、倾听学生回答 学生通过计算写出乙醇的分子式 C2H6O学生推测乙醇可能的结构式:①CH3OCH3;②CH3CH2OH
学生动手插好它们的球棍模型[学生回答]钠过量的原因:保证乙醇完全反应 通过阅读、共同分析讨论“