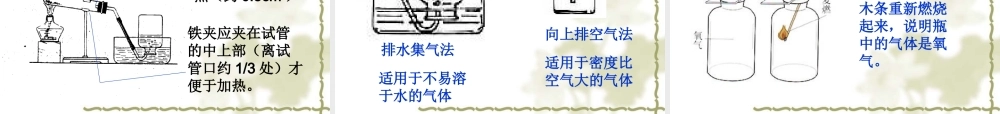
课题 3 制取氧气复习 :1 、如何检验一瓶无色气体是氧气? 把带有火星的木条伸到盛有氧气的集气瓶中,木条重新燃烧起来,说明瓶中的气体是氧气。2 、如何鉴别三瓶无色气体:空气、氧气、氮气? 将燃着的木条分别放入瓶中,如果燃烧得更旺的是氧气;马上熄灭的是氮气;与空气中一样的是空气。一、分解过氧化氢溶液制取氧气1 、试管 中加入过氧化氢溶液,用带火星木条检验; 2 、试管中加入少量二氧化锰后,用带火星木条检验。实验现象:未加入二氧化锰时:加入二氧化锰时:带火星木条不燃烧带火星木条复燃无氧气有氧气过氧化氢 水 +氧气二氧化锰H2O2 H2O O2反应原理:思考: 1 、过氧化氢溶液与二氧化锰反应时,二氧化锰是不是一种反应物?2 、过氧化氢到底是一种什么物质?它在这里起什么作用?实验证明:二氧化锰不是反应物,它只是加快了过氧化氢分解出氧气的速度。二氧化锰时该反应的催化剂 , 起了催化作用。催化剂:在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒)。催化作用:催化剂起的作用叫催化作用。加热氯酸钾和二氧化锰的混合物制氧气二、加热氯酸钾制氧气反应原理: 氯酸钾 氯化钾 + 氧气二氧化锰加热三、加热高锰酸钾制氧气反应原理: 高锰酸钾 锰酸钾 + 二氧化锰 + 氧气加热KClO3 KCl O2KMnO4 K2MnO4 MnO2 O2 氯酸钾 氯化钾 + 氧气二氧化锰加热 高锰酸钾 锰酸钾 + 二氧化锰 + 氧气加热过氧化氢 水 +氧气二氧化锰分析下面三个反应的共同点:分解反应:由一种反应物生成两种或两种以上其他物质的反应,叫做分解反应。AB A+B作业:完成课本 P42 本单元小结内容二、三填空。(可以就做在书上)本课时内容: 实验室制取氧气的反应原理、实验装置、收集方法、注意事项。加热氯酸钾制氧气反应原理: 氯酸钾 氯化钾 + 氧气二氧化锰加热加热高锰酸钾制氧气反应原理: 高锰酸钾 锰酸钾 + 二氧化锰 + 氧气加热KClO3 KCl O2KMnO4 K2MnO4 MnO2 O2加热氯酸钾和二氧化锰的混合物制氧气仪器安装原则:先左后右,先下后上。氯酸钾 + 二氧化锰实验装置实验步骤: 1 、连接好仪器,检查装置的气密性。 2 、把少量氯酸钾和二氧化锰的混合物(或高锰酸钾)装入试管中;并试管口略向下固定在铁架台上。 3 、将集气瓶装满水倒扣在水槽中; 4 、加热试管; 5 、用排水法收集氧气; 6 、将导管从水...