课题课题 2 2 原子的构成原子的构成课题课题 2 2 原子的构成原子的构成第三单元 物质构成的奥秘第三单元 物质构成的奥秘 复习练习:1 、水由 组成, 1 个水分子由 构成
2 、在电解水的实验中,水的 破裂为氢 和氧 ,该反应的文字表达为: ,可见,分子很小,但在化学反应中可以 ,而 在化学变化中不可再分,所以说 是化学变化中的最小的粒子
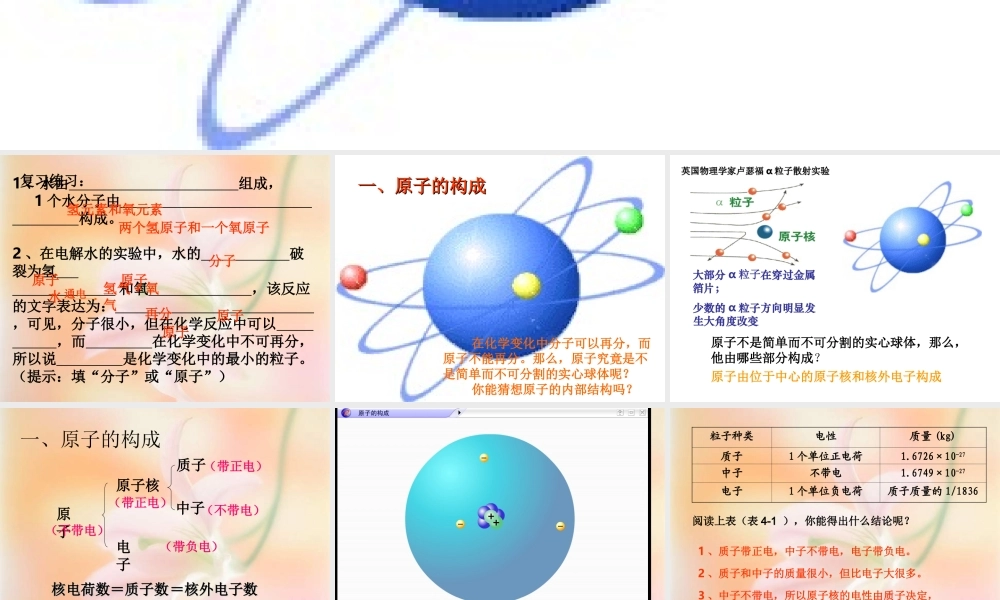
(提示:填“分子”或“原子”) 氢元素和氧元素 两个氢原子和一个氧原子 分子 原子 原子 水 通电氢气 + 氧气 再分 原子 原子 一、原子的构成一、原子的构成 在化学变化中分子可以再分,而原子不能再分
那么,原子究竟是不是简单而不可分割的实心球体呢
你能猜想原子的内部结构吗
原子由位于中心的原子核和核外电子构成 英国物理学家卢瑟福英国物理学家卢瑟福 αα 粒子散射实验粒子散射实验大部分 α 粒子在穿过金属箔片;少数的 α 粒子方向明显发生大角度改变原子不是简单而不可分割的实心球体,那么,他由哪些部分构成
一、原子的构成原 子电 子原子核质子中子(带正电)(不带电) (带负电) (带正电)(不带电) 核电荷数=质子数核电荷数=质子数表 4-1表 4-2示 例=核外电子数=核外电子数练 习 粒子种类电性质量 (kg)质子1 个单位正电荷1
6726×10-27中子不带电1
6749×10-27电子1 个单位负电荷质子质量的 1/1836阅读上表(表 4-1 ),你能得出什么结论呢
1 、质子带正电,中子不带电,电子带负电
2 、质子和中子的质量很小,但比电子大很多
3 、中子不带电,所以原子核的电性由质子决定, 因此原子核带正电,数目跟质子相等
原子种类 质子数 中子数核外电子数氢101碳666氧88 8钠111211氯171817铁263026观察表格(表 4-2 ) ,思考下列问题2 、所有原子都是由质子、中子、电子构成