复习提问 什么叫溶质质量分数
说出它的计算公式 溶质质量溶液质量×100%溶质的质量分数=或=溶质质量溶质质量 + 溶剂质量×100%计算公式:定义:溶质的质量与溶液的质量之比
〖例 1 〗从一瓶氯化钾溶液中取出 20 克溶液,蒸干后得到 2
8 克氯化钾固体
试确定这瓶溶液中溶质的质量分数
解:这瓶溶液中溶质的质量分数为:答:这瓶溶液中氯化钾的质量分数为 14%
8g20g ×100%= 14%1 .有关溶液的基本计算 练习 :1
下列说法是否正确
( 1 ) 100 ㎏水中加入 20 ㎏ NaCl ,溶液中溶质的质量分数为 20 %( 2 ) 25℃ 时,向 100 克溶质质量分数为 5 %的 NaCl 溶液中加入 5 克 KCl ,完全溶解后,溶液中 NaCl 的质量分数不变 2
把 50 克 NaNO3 溶液蒸干后,得到 10 克 NaNO3 ,求原溶液中溶质质量分数3
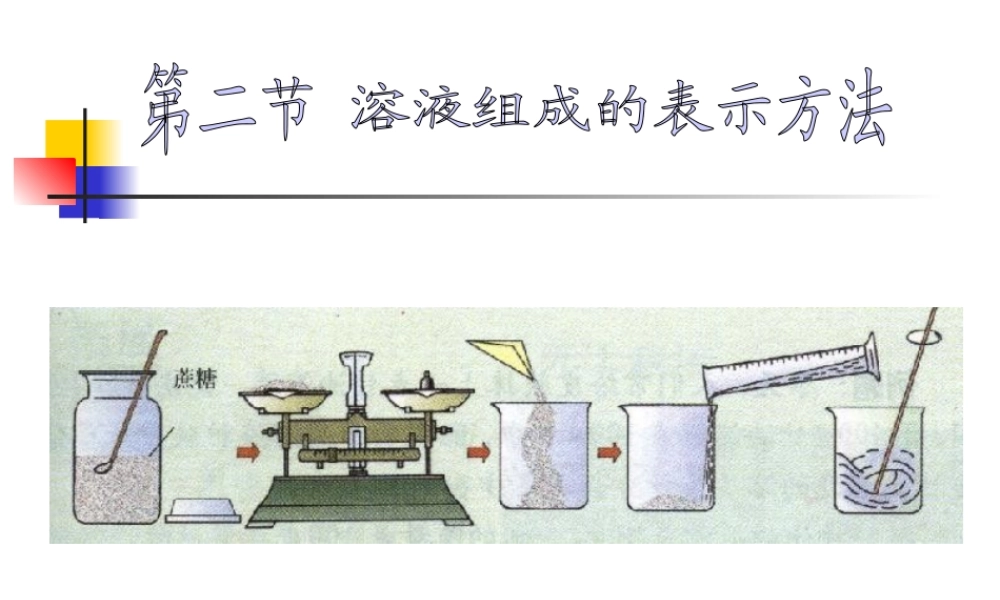
现有 80 克溶质质量分数为 10 %的 KNO3 溶液 , 向其中加入 20 克 KNO3 ,完全溶解后,求溶液中溶质质量分数 配制 100 克溶质质量分数为 10 %的 NaCl 溶液,如何操作
步骤: 1
溶解 三.有关溶液的稀释(或浓缩)例: 100g10% 的食盐水向其中加入 100g 水后,其溶质质量分数是多少
设:设加水后溶质质量分数为 x稀释前后溶质质量不变
100g×10% = ( 100g+100g ) x稀释前溶液中所含溶质稀释后溶液中所含溶质X=5%答:加水后溶质质量分数为 5% 小结:溶液稀释前后溶质的质量不变稀溶液的质量 = 浓溶液的质量 + 稀释所用水的质量 练习:1
有 50g 溶质质量分数为 20% 的 NaCl 溶液,要把它变成 10% 的食盐水,需加水多少克
取 98% 浓硫酸 20