初高中化学衔接复习资料基本概念和理论一、物质的组成和结构(一)物质的组成(二)化合价和原子团1.化合价(1)定义:一种元素一定数目的原子跟其他元素一定数目的原子化合的性质,叫做这种元素的化合价
(2)实质:化合价是元素的化学性质
(3)常见元素及原子团的化合价: 化合价有正价和负价,化合物中正、负化合价代数和为零
单质中元素的化合价为零
在带电原子团中,正、负化合价代数和不为零,代数和为原子团的化合价
(注意:①同一元素,在不同的原子团中,可显相同的化合价;如:CrO42— Cr2O72—② 同一元素,在结构相同的原子团中,可显不同的化合价;如: KMnO4 K2MnO4③ 同一元素,在同一物质中,可显不同的化合价
如:NH4NO3)化合价口诀一价 钾 钠 银 铵 氢,二价 钙 镁 钡 铅 锌; 三五价有 磷 和 氮 ,四价 硅 锰 还有 碳 ; 一二 铜 汞 二三 铁,铝 是三价要记得; 四六负二 硫 出现,氧是负二经常见
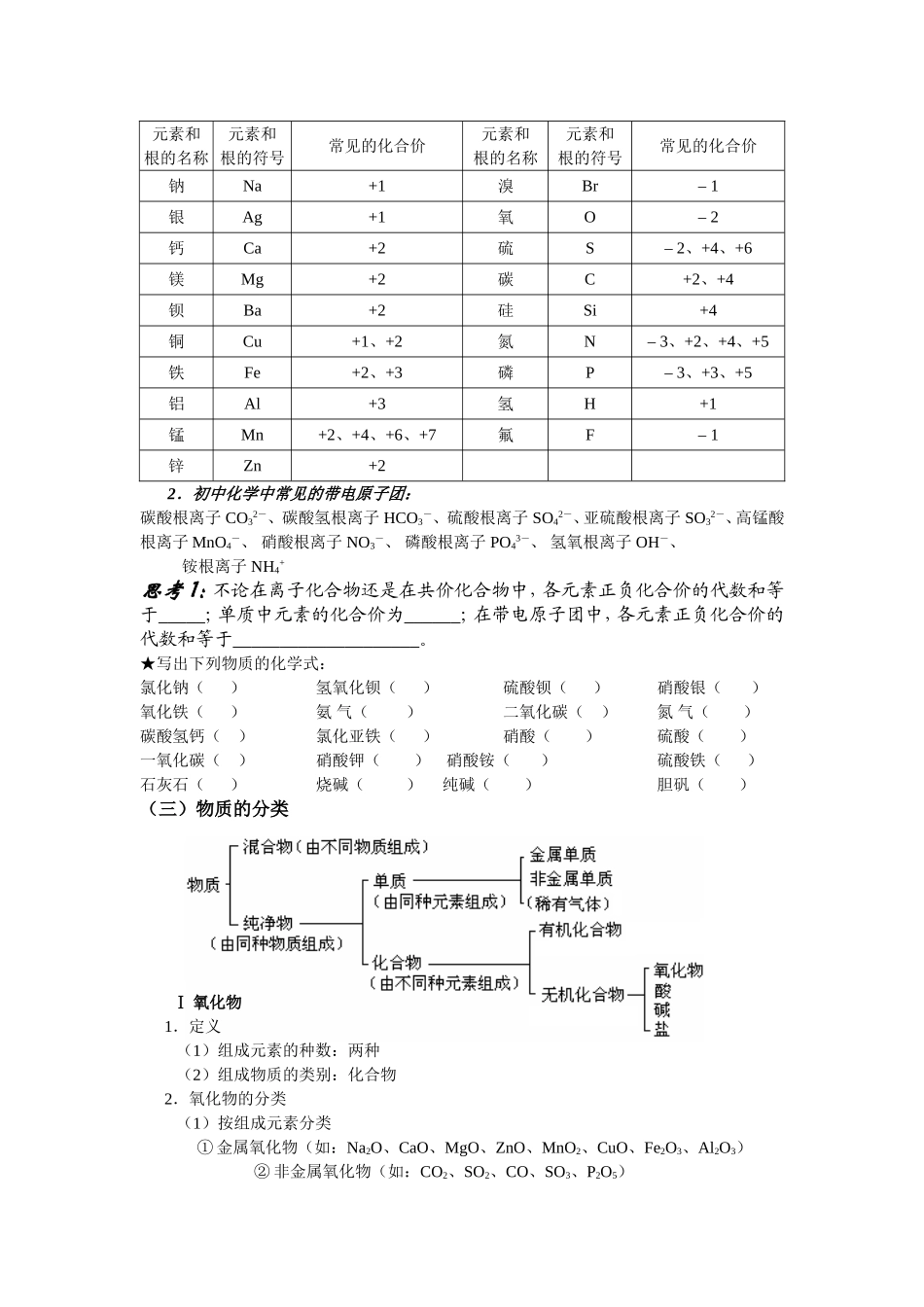
一些常见元素的化合价元素和根的名称元素和根的符号常见的化合价元素和根的名称元素和根的符号常见的化合价钾K+1氯Cl – 1、+1、+5、+7质子中子构成原子核电 子构成原子( 直接 ) 构成物质组成元素离子分子构成变成构成构成(纯净物)单质化合物同种元素成组 不同元素组 成元素和根的名称元素和根的符号常见的化合价元素和根的名称元素和根的符号常见的化合价钠Na+1溴Br– 1银Ag+1氧O– 2钙Ca+2硫S– 2、+4、+6镁Mg+2碳C+2、+4钡Ba+2硅Si+4铜Cu+1、+2氮N– 3、+2、+4、+5铁Fe+2、+3磷P– 3、+3、+5铝Al+3氢H+1锰Mn+2、+4、+6、+7氟F– 1锌Zn+22.初中化学中常见的带电原子团:碳酸根离子 CO32-、 碳酸氢根离子 HCO3-、 硫酸根离子 SO42-、亚硫酸根离子 SO32-、