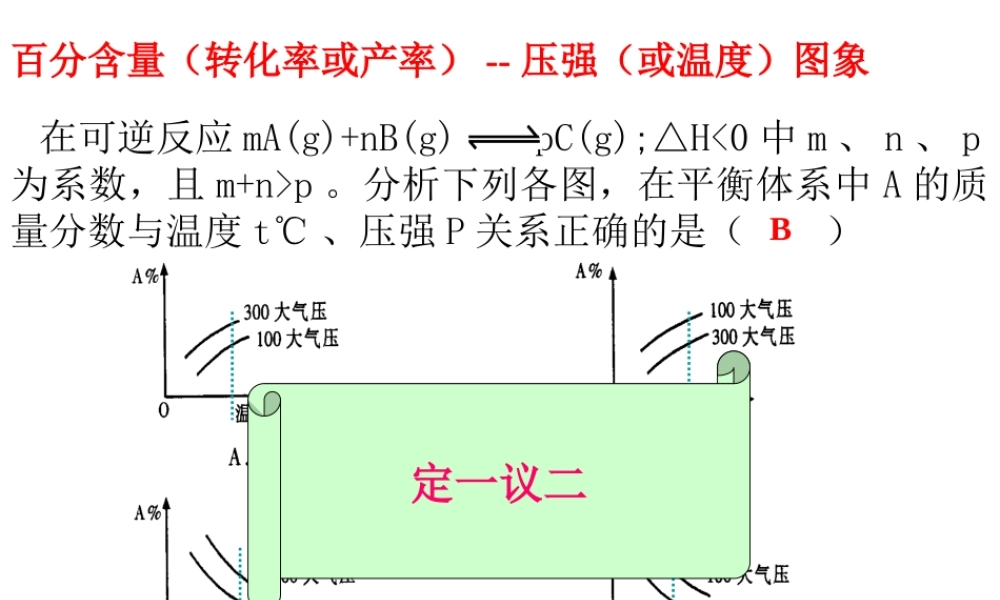
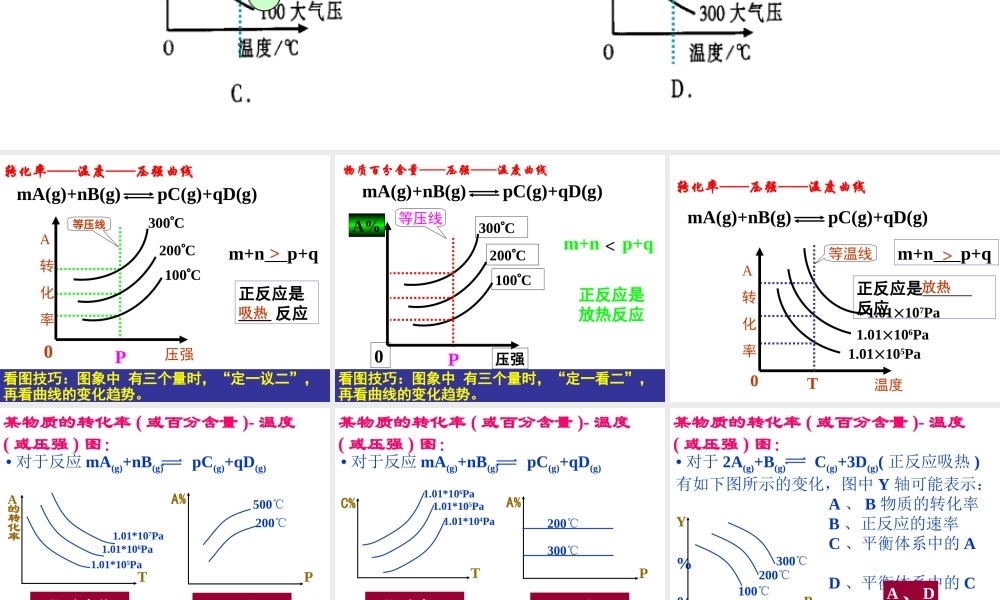
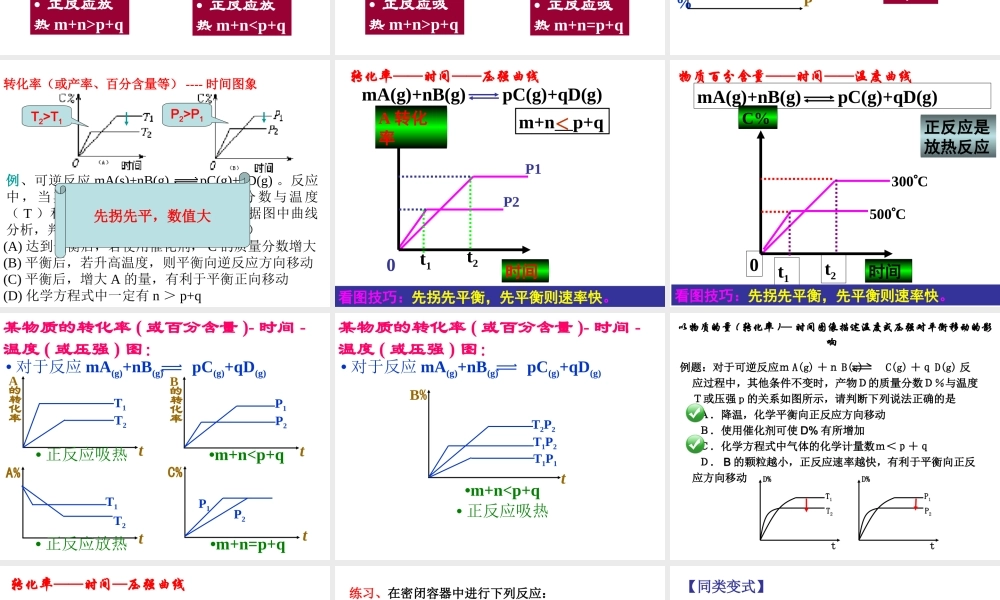
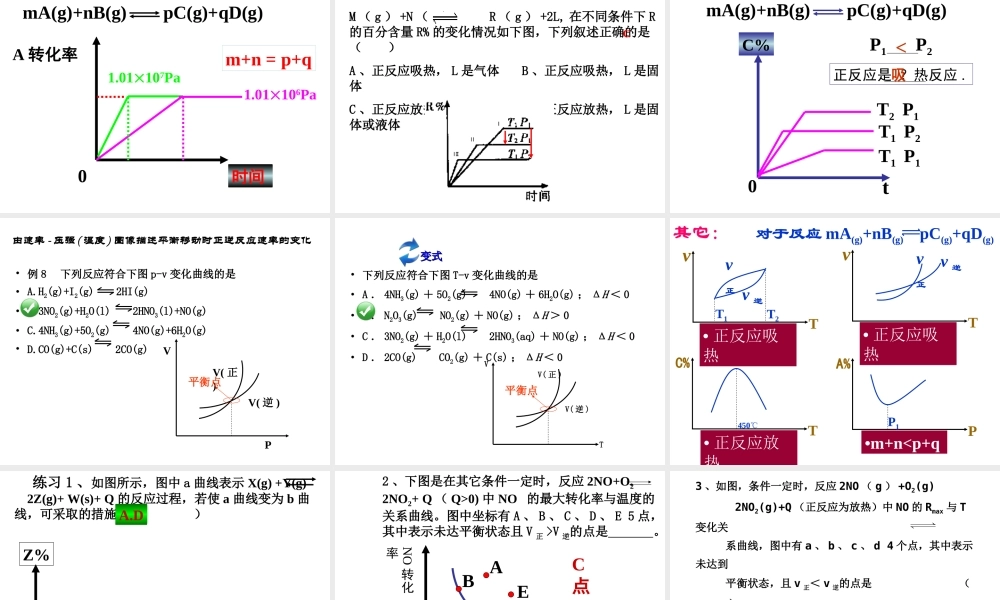
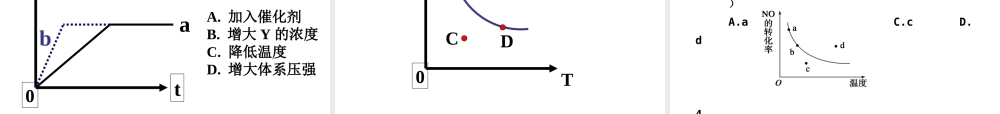
在可逆反应 mA(g)+nB(g) pC(g);△Hp
分析下列各图,在平衡体系中 A 的质量分数与温度 t℃ 、压强 P 关系正确的是( )百分含量(转化率或产率) -- 压强(或温度)图象B定一议二 mA(g)+nB(g) pC(g)+qD(g)200C300C100CA转化率压强0Pm+n p+q>正反应是____ 反应看图技巧:图象中 有三个量时,“定一议二”,再看曲线的变化趋势
等压线转化率——温度——压强曲线吸热 200C300C100CmA(g)+nB(g) pC(g)+qD(g)Pm+n p+q正反应是 反应等温线放热 PA%500℃200℃某物质的转化率 ( 或百分含量 )- 温度( 或压强 ) 图:• 对于反应 mA(g)+nB(g) pC(g)+qD(g)TA的转化率1
01*107Pa1
01*106Pa1
01*105Pa• 正反应放热 m+n>p+q• 正反应放热 m+np+qPA%300℃200℃• 正反应吸热 m+n=p+q 某物质的转化率 ( 或百分含量 )- 温度( 或压强 ) 图:• 对于 2A(g)+B(g) C(g)+3D(g)( 正反应吸热 )有如下图所示的变化,图中 Y 轴可能表示: A 、 B 物质的转化率 B 、正反应的速率 C 、平衡体系中的 A% D 、平衡体系中的 C%PY100℃200℃300℃A 、 D (A) 达到平衡后,若使用催化剂, C 的质量分数增大(B) 平衡后,若升高温度,则平衡向逆反应方向移动(C) 平衡后,增大 A 的量,有利于平衡正向移动(D) 化学方程式中一定有 n > p+q例、可逆反应 mA(s)+nB(g) pC(g)+qD(g)
反应中,当其它条件不变时, C 的质量分数与温度( T )和压强( P )的关系如上图,根据图中曲线分析,判断下列叙述中正确的是( )B转化率(