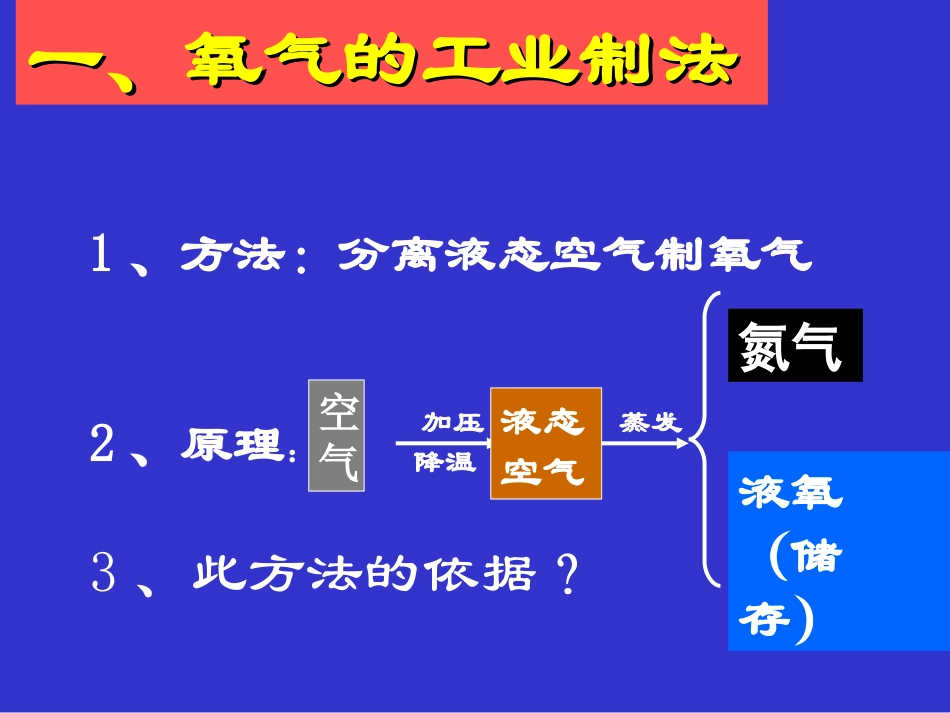
氧气的制法一、氧气的工业制法一、氧气的工业制法1、方法:分离液态空气制氧气加压2、原理:降温液态空气蒸发氮气液氧(储存)3、此方法的依据?什么变化?空气二、实验室制法二、实验室制法方法三:加热氯酸钾(加入二氧化锰)方法一:加热高锰酸钾方法二:常温分解过氧化氢溶液(加入二氧化锰)思考:思考:1、加热高锰酸钾或氯酸钾制氧气需要哪些仪器?发生装置收集装置加热高锰酸钾制取氧气装置图棉花查装定点收移熄6、实验步骤制取装置收集装置组、查、装、定、点、收、离、熄①3、操作步骤组装仪器(从左向右、从下往上)②检查装置气密性③装药品(把药品平铺在试管底部)④固定装置⑤加热(用酒精灯的外焰加热、先预热,再集中在盛药品处加热)⑥收集氧气(当气泡连续并均匀地放出时开始收集)⑦从水槽中移出导管⑧熄灭酒精灯排水法:一.适用范围不易溶于水的气体二.优点1.易于收集到较纯的气体2.便于观察气体是否已经收集满4、收集方法:向上排空气法一.适用范围密度比空气大的气体二.优点操作较为方便5、验满方法排水法:当集气瓶的一侧有气泡放出时,证明已收集满向上排空气法:将带火星的木条放在集气瓶口,若木条复燃,证明已收集满。6、放置方法:正放在桌子上,并盖上毛玻璃片注意事项注意事项4、用高锰酸钾高锰酸钾制氧气时,要在试管口塞团棉花?1、试管口略向下倾斜防止水倒流炸裂试管2、铁夹位置?距管口1/3处3、伸入试管的导管不宜过长,刚露出塞子即可防止高锰酸钾粉末进入导管。注意事项注意事项5、加热时,先_____,然后固定在______________加热6、排水法时,导气管刚过集气瓶口;排空气法则需插入集气瓶底;7、收集气体时候?气泡连续均匀冒出时预热放药品的部位注意事项注意事项8、实验结束时,先撤______,后撤_______。导管酒精灯防止水槽里的水倒流到试管里,炸裂试管指出下图中的四处错误3、试管口应略向下倾斜4、试管口应略低于试管底1、应用外焰对准药品加热2、导气管应与橡皮塞齐平二、实验室用过氧化氢制氧气1、药品:反应物:过氧化氢(无色液体)催化剂:二氧化锰(黑色粉末)2、原理:二氧化锰二氧化锰水水++氧氧气气过氧化氢过氧化氢HH22OO22HH22OOOO22MnO2催化剂:在化学反应中能增大增大化学反应速率,而本身的质量质量和化学性质化学性质在化学反应前后都没有改变的物质叫做催化剂。催化剂特点:一大:二不变:增大其它物质的反应速率本身的质量化学性质化学反应前后不变催化作用:催化剂在化学反应中所起的作用叫催化作用。实验步骤1:组装仪器使用长颈漏斗时,长颈漏斗的末端必须插入液体中,防止生成的气体从长颈漏斗口逸出,所以必须液封。2、检查装置气密性3、加药品用止水夹夹住橡皮管,然后从长颈漏斗注入水,等一段时间,若长颈漏斗内能形成一段比锥形瓶内液面高的水柱,证明气密性良好1、过氧化氢(二氧化锰)制取氧气装置(固液常温型装置)二氧化锰二氧化锰过氧化氢水+氧气1、在上图所示装置中,使用了哪些仪器?2、哪部分是气体发生装置,哪部分是气体收集装置?注意:使用长颈漏斗时,长颈漏斗的末端必须伸入液面以下,防止生成的气体从长颈漏斗口逸出。(导管不能伸入液面以下)说明:装置1简单装置2可以随时添加液体装置3可以控制反应速率氯酸钾二氧化锰氯化钾+氧气加热KClO3KClO2H2O2H2O+O2MnO2气体发生装置固体加热液体不需要加热气体收集装置+发生装置收集装置+实验装置的比较过氧化氢加入二氧化锰制氧气比用高锰酸钾加热制氧气有哪些优点?(1)常温反应,不需加热(或操作简便);(2)反应速率快;(3)环保,无污染物质产生。反应物都是固体,反应需要加热反应物是固体和液体的混合物,反应不需要加热固液常温型固体加热型制取气体的发生装置A_______B_______C_______D_______E_______F_______试管铁架台酒精灯导管集气瓶水槽发生装置收集装置ABCDEF实验室制取气体的一般思路是什么?小结:根据反应原理选择原料根据反应物状态和反应条件选择制气装置根据生成气体的性质(物理)选择收集装置操作方法、检验、验满方法等固体加热型固液常温型复习:1、实验室制取氧气有哪些反应:氯酸钾KClO3氯化钾+氧气二氧化锰加热...