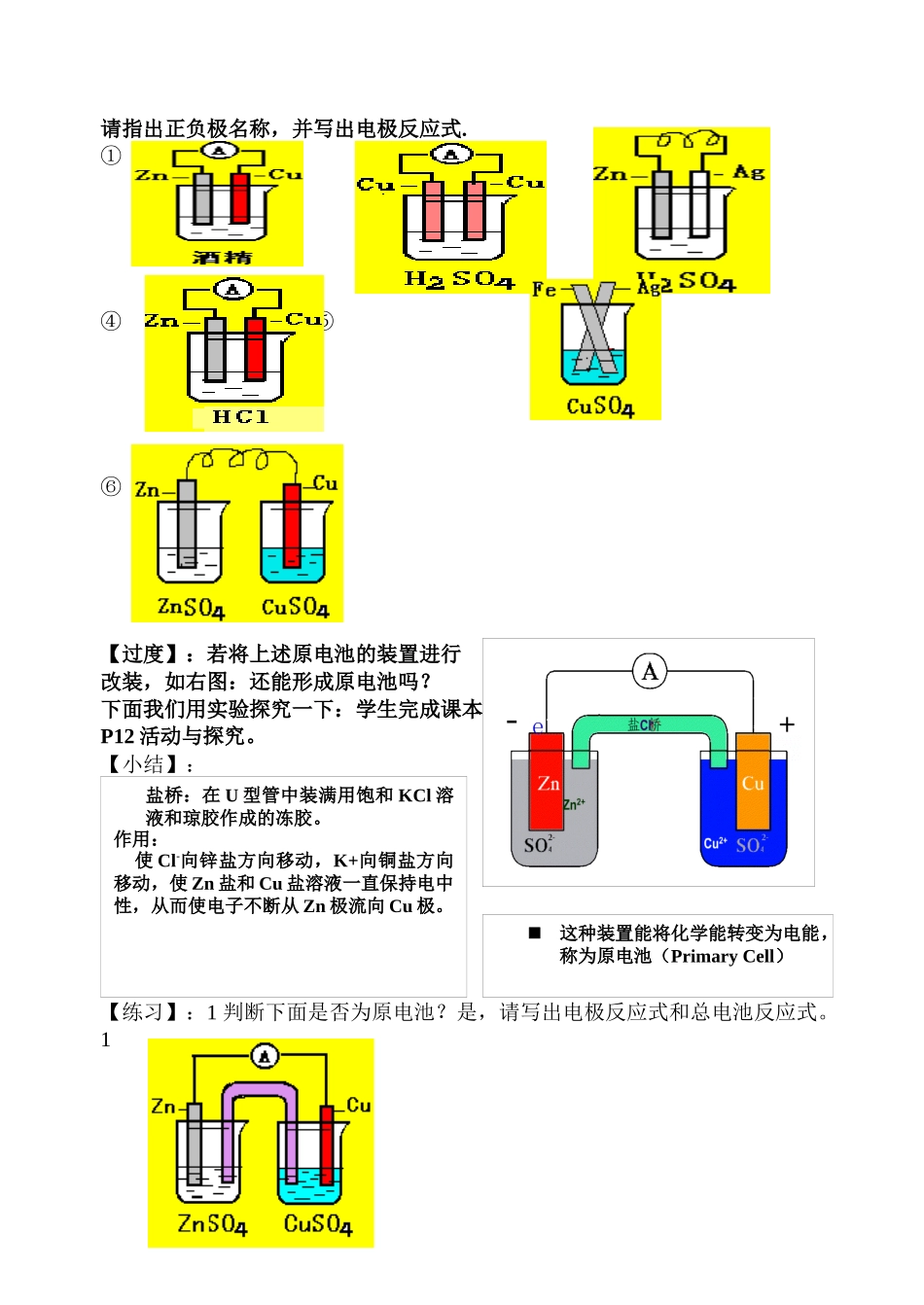
《原电池的原理》教学案 [教学目标]知识与技能:复习巩固原电池的构成条件、工作原理,通过进行化学能转化为电能的探究活动和一系列设计制作原电池的活动,更深刻地认识原电池的构造特点和工作原理,更熟练正确地书写电极反应式
过程与方法:学生动脑设计、动手制作各种原电池,同一实验小组成员间的相互协作,不同组间相互竞争,提供展示作品的舞台,极大地调动了学生的学习积极性,并在愉快的活动中更深刻地认识原电池的构造特点和工作原理
情感、态度、价值观:让学生在设计活动中体味到知识的力量,运用知识可以改善我们的生活质量,造福人类
[重点]:各种原电池的设计和电极方程式的书写[难点]:原电池的构成条件,各种原电池的设计和电极方程式的书写及相关计算 [实验用品]:溶液:1mol/L CuSO4溶液、1mol/LZnSO4溶液、1mol/LH2SO4溶液、1mol/LNaOH 溶液、1mol/LFeCl3溶液、1mol/LNaCl 溶液、酒精电极材料:Fe 棒 1 根、Cu 棒 1 根、C 棒 2 根、Zn 片 2 片、Cu 片 2 片、Mg 条两条、Al 条 1 条其它:灵敏电流计、导线两根、夹子两个,250ml 烧杯 1 个、小塑料水槽四只胶头滴管、洗瓶、塑料盆(废液缸)、抹布、砂纸[教学过程]:【知识回顾】:电化学:指研究化学能与电能之间相互转换的装置、过程和效率的科学
按电化学反应过程及装置分:1
产生电流的化学反应及装置 (如:原电池等)2
借助电流而发生反应及装置 (如:电解池)一、原电池1 什么是原电池
构成原电池的条件是什么
【学生答】:(1)有两个相连的电极: a 导体; b 相连的形式可以多种多样的;(可以用导线相连,也可以两个电极相接触) c 电极材料可以多种多样
两种活泼性不同的金属
电极本身都参与反应吗
一种金属与一种非金属(如石墨)